Epidemiological survey of a case caused by highly variant vaccine-derived poliovirus in Hubei
YANG Bei-fang1, LI Shu-hua1, LIU Na1, SHU Duan2, DENG Zhen-gang2
Hubei Provincial Center for Disease Control and Prevention, Wuhan 430079, Hubei, China
Abstract
Objective To understand the epidemiological characteristics of a case caused by highly variant vaccine derived poliovirus in Hanchuan, Hubei province, in May 2013. Methods The case survey, virus excretion monitoring, laboratory examination and transmission risk assessment were conducted and the case was isolated and followed up. Results The isolate from the case was identified as highly variant vaccine-derived poliovirus type Ⅲ(8nt, 0.88%) by nucleotide sequencing in provincial and national polio laboratory, respectively. The case had received irregular 2 dose oral polio vaccine (OPV) immunization. Conclusion The case was finally diagnosed with non-acute flaccid paralysis (AFP) and no further transmission occurred due to strict prevention and control measures, including active search for AFP cases and supplementary immunization of OPV among the local children.
湖北省一例脊髓灰质炎疫苗高变异株病例的流行病学调查分析
杨北方1, 李书华1, 刘娜1, 舒端2, 邓振刚2
1. 湖北省疾病预防控制中心, 湖北 武汉 430079;
2. 汉川市疾病预防控制中心
2. 汉川市疾病预防控制中心
摘要
目的 阐述湖北省1例脊髓灰质炎(脊灰)疫苗高变异株病例的流行病学调查与处理情况。 方法 对疫情开展病例个案调查、实验室检测、病毒传播风险评估,对病例进行消毒、随访,由省级AFP病例专家诊断小组会诊并做出临床分类。 结果 2013年5月,湖北省发生1例Ⅲ型脊灰疫苗高变异株病毒病例,经省级和国家脊灰实验室在对病例所分离到的脊灰病毒进行核苷酸序列测定时,与Sabin疫苗株比较发现VP1区有8个(0.88%)核苷酸变异。患儿总共口服了2剂次脊灰减毒活疫苗(oral poliomyelitis vaccine, OPV),未规范服苗。 结论 该病例最终分类诊断为非AFP病例。各级卫生部门采取了包括主动搜索急性弛缓性麻痹(acute flaccid paralysis, AFP)病例、开展查漏补种OPV等措施,有效控制了疫情的扩大和蔓延。
内容大纲
1 资料与方法
1.1 资料来源 湖北省疾病预防控制中心(CDC)调查小组赴现场进行流行病学调查结果,省级脊灰实验室及国家脊灰实验室的检验结果,患儿临床检查报告及体检记录,省级和国家级AFP专家诊断小组结论等资料。
1.2 现场调查方法
1.2.1 病例个案调查
通过现场调查了解患儿基本情况、免疫史、接触史、就诊史、居住环境等情况。
1.2.2 病例排毒检测
再次采集患儿至少间隔24 h的粪便标本2份,并同时采集周围密切接触儿童11人的粪便标本13份,所有粪便标本及时送湖北省CDC脊灰实验室进行病毒分离与鉴定。
1.2.3 病毒传播风险评估
1.2.3.1 医院AFP病例主动搜索
对汉川市(县级市)的AFP监测医院(市人民医院)进行AFP病例主动搜索,搜索从2011年1月1日至2013年5月11日搜索当日所有AFP 病例,调查有无AFP漏报病例的发生。
1.2.3.2 社区疑似AFP病例主动搜索
对患儿所在村组和周边村组进行疑似AFP病例的主动搜索,通过询问乡村医生、村民和学校老师,了解患儿发病前后2个月内本村和学校学生是否有患相似临床症状和体征的病例出现。
1.2.3.3 OPV查漏补种
对患儿所在乡和相邻乡镇所有2月龄至6岁儿童进行OPV查漏补种工作,通过询问和查看每名儿童的预防接种证,了解脊灰疫苗接种情况,发现漏种则现场予以补种1剂次OPV。
1.3 实验室检测方法
湖北省CDC脊灰实验室按照要求进行病毒分离鉴定,并对阳性分离物开展核苷酸序列测定,同时送国家脊灰实验室做测定以便确认。
2 结果
2.1 现场调查情况患儿李某,男,汉族,2005年4月12日出生,户籍地址为湖北省孝感市汉川市某农村。汉川市CDC于2013年3月30日和31日分别采集2份合格粪便标本,4月1日送到湖北省CDC脊灰实验室进行病毒检测。5月7日,经湖北省CDC脊灰实验室进行肠道病毒分离培养,检出Ⅲ型脊灰病毒,对阳性标本进行了核苷酸序列测定;并于5月9日送阳性标本到国家脊灰实验室进行核苷酸序列测定。5月10日湖北省CDC脊灰实验室报告了核苷酸序列测定结果,该标本Ⅲ型脊灰病毒与昆明株比较有7个核苷酸序列变异,病毒变异率为0.77%,与Sabin疫苗株比较有8个核苷酸序列变异,病毒变异率为0.88%,未达到VDPV标准,属于Ⅲ型脊灰疫苗病毒高变异株,遂开展相关调查。5月15日,国家脊灰实验室反馈核苷酸序列测定结果,与湖北省一致。
2.1.1 病例就诊及报告情况
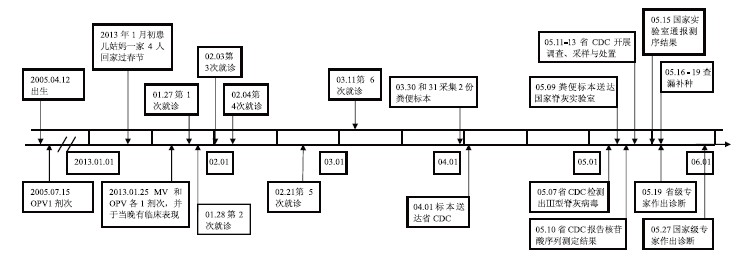
患儿在2013年1月25日进行了麻疹疫苗和脊灰疫苗接种,并于当晚出现抽动症状,无发热、腹泻、颈项强直,无3日内注射史。随后,患者于1月27日到汉川市人民医院内科就诊,诊断为抽搐待查和神经炎。1月28日到武汉市儿童医院就诊,诊断为抽动症,其中脑电图检查显示正常儿童清醒脑电图,MRI检查示颅脑MRI扫描未见明显异常征象,右侧筛窦轻度炎症。主要治疗药物为泰必利片、肌苷片等。2月3日到湖北省妇幼保健院内科就诊,初步诊断为抽动症和中枢神经系统感染,并建议转小儿神经康复科就诊。2月4日湖北省妇幼保健院小儿神经康复科专家诊断为抽动综合征。治疗药物为硫必利、肌苷。2月21日到省妇幼保健院复诊,患儿症状缓解,查脑电图、脑电地形图检查示正常范围儿童清醒脑电图,脑电地形图各频带分布及功率无异常,并按抽动症继续予以治疗。3月11日到武汉市儿童医院神经内科复诊,诊断与用药同前。见图1。
2.1.2 接触史
2013年1月底2月初,李某表妹(刘某,2008年11月20日出生)一家4人从云南省昆明市回到外婆家过春节,刘某父母和弟弟年后返回云南省,而刘某一直居住在李某家,刘某已按免疫程序接种3剂脊灰疫苗,时间分别是2009年1月22日、2月20日和3月20日。李某妹妹(2011年2月10日出生)接种脊灰疫苗5剂次(常规免疫3剂,分别是2011年4月10日、5月10日和6月10日;强化免疫两剂次时间为2012年12月5日和2013年1月25日)。目前,2名家庭内密切接触儿童均无类似或迟缓性麻痹症状,身体健康。患儿在此期间多次接触同村村民及儿童。该户与村医只隔一家,该村基本每户一个户外厕所。
2.1.3 免疫预防情况
在乡镇卫生院查验接种簿/卡,并在村内查看了接种证,该患儿于2005年7月15日、2013年1月25日各接种1剂脊灰疫苗,共2剂OPV。据患儿家长及爷爷奶奶回忆该病例除了这两次服用过OPV外无其他时间服用过OPV的印象。由于家属不同意,未对患儿采血进行脊灰抗体水平检测。该患儿其他疫苗常规免疫也没有完成,漏种、不及时接种很多,据家属介绍是无故未种。
图1 患儿出生、服苗、发病就诊及诊断经过
Figure 1 Process of birth, vaccination, sick, diagnose and treatment of the case
2.1.4 居住环境情况
患儿全家居住于2层的楼房内,院内卫生条件一般,用水从周围院内打取,污水直接泼洒到院外,院外25 m处有户外厕所。除在武汉市就诊外其余时间在家里居住,无其他外出史。
2.2 排毒监测情况
共采集11名密切接触者粪便标本,其中患儿及家庭内2名密切接触者分别采集2份,其余9名密切接触者分别采集1份粪便标本,所有15份标本肠道病毒分离结果均为阴性。
2.3 病毒传播风险评估
2.3.1 医院AFP病例主动搜索
对汉川市人民医院儿科、神经内科、康复科、病案室等重点科室的门诊和住院登记情况进行了医院AFP病例主动搜索,病案室搜索范围为2011年1月1日至搜索当日存档病历,无漏报病例。核查4842例相关科室出入院登记住院病例,无AFP病例。对保健科AFP监测记录进行了核对,自2013年以来共上报3例AFP病例,均已录入并上报AFP监测信息报告管理系统。
2.3.2 社区AFP病例主动搜索
在开展查漏补种工作同时,分别对杨林沟镇(总人口数45 946人)和湾潭乡(总人口数26 096人)进行了AFP病例社区主动搜索,未发现疑似病例。
2.3.3 OPV查漏补种
病例发生后,汉川市CDC迅速安排部署脊灰疫苗查漏补种工作,于5月13日下午召开查漏补种工作动员会,于14-15日对杨林镇、湾潭乡适龄儿童开展摸底调查,于16-19日在杨林沟镇30个村和湾潭乡21个村开展2月龄至6岁儿童的OPV查漏补种,即为2007年1月1日以后出生的儿童,无免疫史或未全程免疫或免疫史不详,不管其居住地与出生地,只要没有接种禁忌证,一律按要求补齐接种针次,即4岁以下要求接种3针次基础免疫,4岁以上接种4针次(基础免疫3针次+加强免疫1针次)。重点为外出打工返乡人群儿童,行政上难以区分的本地区儿童和流动儿童。两地共登记儿童总数为3264人,其中应接种儿童 453人,实种儿童448人,接种率98.90%,0~3岁应补种83人,实种82人,接种率98.80%;4岁及以上应种370人,实种366人,接种率98.92%。其中杨林沟镇共登记儿童总数为1940人,其中应种儿童106人,实种儿童106人,接种率100.00%。湾潭乡共登记儿童总数为1324人,其中应种儿童347人,实种儿童342人,接种率98.56%。常规免疫儿童未种原因包括接种时有禁忌证、家长拒绝接种等情况。
2.4 控制措施
在对患儿进行粪便排毒情况检测和随访期间,建议患儿减少外出,居家隔离,每日对患儿排泄物及居住环境消毒。
2.5 专家诊断小组意见
5月19日,湖北省AFP病例专家诊断小组对该病例首先临床诊断为抽动综合征,其次诊断排除为非AFP病例,与本次接种脊灰疫苗、麻疹疫苗无因果关联。5月27日,中国CDC召开讨论会,与会专家同意湖北省专家的诊断结论。
2.6 随访
湖北省CDC于8月9 10日再次派专家对该患儿进行了随访,患儿已经恢复正常,学校和村庄周围乡镇无脊灰疫苗相关病例发生。
3 讨论
3.1 临床分类不符合AFP病例定义和不属于国际疾病分类(international classification of diseases, ICD) ICD-10中AFP监测病例的14个种类。最初患儿于1月25日口服一剂脊灰疫苗并接种一剂麻疹疫苗,服苗后当天晚上出现抽动症状,随后到汉川市人民医院就诊,并多次到武汉市和湖北省妇幼保健院就诊,然后临床诊断患儿为抽动综合征。发病后未再服用OPV,仅于服苗后2个月的首次送检粪便标本中分离到脊灰疫苗Ⅲ型病毒,且病毒VP1 区变异<1%,分类诊断为高变异株病毒病例。最终,省级AFP病例分类专家诊断小组对该例患儿进行分类,并确定为非AFP病例,随后国家级专家讨论后同意省级专家结论。
3.2 脊灰疫苗株病毒来源
综合考虑患儿所感染脊灰病毒来源主要有四种可能:(1)与周围强化免疫对象,特别是与家庭内强化免疫对象的密切接触导致感染病毒。(2)由于当地在2012年12月5 6日和2013年1月5 6日开展了两轮脊灰疫苗强化免疫,农村卫生条件较差,强化免疫对象很有可能排毒到周围外环境中,患儿通过污染的水、土等外环境感染病毒。(3)云南省回来过年的亲戚带病毒从而感染病例。(4)外环境中早就存在脊灰疫苗株病毒,病毒可能发生变异或者重组,导致致病性增强,患儿从外环境中感染 。另外,患儿服苗后2个月采集粪便标本,病毒分离后测序结果显示Ⅲ型病毒VP1区有7个碱基变异,根据每个位点大约每年1%的变异速率推断 ,疫苗病毒在短时间还不足以产生如此大的变异。因此,根据该病例的流行病学史、临床症状体征和检查以及病原学检测结果还不能诊断为疫苗相关病例。
3.3 防控措施
脊灰潜伏期为3~6 d,从感染到麻痹发生一般7~12 d,范围3~35 d。在此期间患儿居住在汉川市。根据基因位点大约每年1%的变异速率推断,变异病毒已在环境中至少存在半年,有继续传播的可能。建议当地CDC及时开展患儿周围外环境消毒等措施消灭传染源。调查中了解到当地仍存在流动儿童、服苗期间有禁忌证而导致延迟接种儿童等其他免疫空白人群,有必要迅速开展接种率调查,了解当地免疫工作实际情况。有研究指出只有高的OPV接种率才能够有效保护儿童免受脊灰野病毒、疫苗衍生病毒的侵袭并且阻断其循环[14],因此应进行OPV的查漏补种,必要时开展强化免疫工作,避免病毒传播甚至进一步变异引起VDPV及其循环事件(cVDPVs),但这也正是OPV的无法克服的缺点[15]。
本次OPV查漏补种工作结果显示,当地儿童脊灰疫苗常规免疫漏种剂次达到了13.88%,至少说明两乡镇的脊灰疫苗漏种现象较严重。另外,本次查漏补种脊灰疫苗漏种率为1.10%,反映此次查漏补种工作效果很好。AFP病例主动搜索结果表明AFP监测系统敏感,且患儿已停止排毒,因此本次疫情传播风险基本排除。总的来说,通过本次调查,汉川市应加强针对留守儿童、流动儿童及其家属的宣传教育,做好常规免疫、强化免疫、查漏补种及学校查验预防接种证工作,消除局部免疫空白,建立牢固的免疫屏障。
患儿自发病以来在汉川市和武汉市几家医院间进行治疗,病例的调查处理由湖北省CDC、汉川市CDC进行。高变异株病例有别于高危和聚集性AFP病例,具有较明确的致病性和传播性。为了达到阻断病毒传播控制疫情的目的,今后各级CDC需要从加强人员培训,提高AFP监测的敏感性和及时性,开展脊灰疫情应急演练,提高人员疫情处置能力着手做好维持无脊灰状态工作。
参考文献
[1] WHO. Major Milestone Reached in Global Polio Eradication: Western Pacific Region is Certified Polio-Free. http://www.who.int/inf-pr-2000/en/pr2000-71.html.
[2] WHO. Circulating vaccine-derived poliovirus1 (cVDPV) 2000-2013. http://www.polio eradication.org/ Data and monitoring/Polio this week/Circulating vaccine derived poliovirus.aspx.
[3] Zhu SL, Zhang Y, Yan DM, et al. Running status and evaluation of Chinese polio laboratories network in 2009 [J]. Chinese Journal of Vaccines and Immunization,2013,19 (3):204-209. (in Chinese) 祝双利,张勇,严冬梅,等.中国2009年脊髓灰质炎实验室网络的运转情况与评价[J].中国疫苗和免疫,2013,19(3):204-209.
[4] Liu DQ, Zhao YP, Chen XQ, et al. Surveillance and epidemiology of cases caused by vaccine derived poliovirus in Anhui province[J]. China Journal of Vaccines and Immunization,2004,10(6):333-335. (in Chinese) 刘丹青,赵月萍,陈晓琴,等.安徽省疫苗变异脊髓灰质炎病毒病例的监测及其流行病学分析[J].中国计划免疫,2004,10(6):333-335.
[5] Zhang H, Xu XY, Chen YW, et al. A case caused by vaccine derived poliovirus typeⅡ[J]. Preventive Medicine Tribune,2007,13(6):2,485. (in Chinese) 张宏,许旭艳,陈杨伟,等.1例Ⅱ型脊髓灰质炎病毒疫苗变异株病例[J].预防医学论坛,2007,13(6):封2,485.
[6] Zhang ZG, Chen M, Guo Y, et al. Variation in poliovirus nucleotide in AFP cases in Hebei province,2007-2008[J]. Journal of Preventive Medicine Information,2009,25 (12) :1020-1022. (in Chinese) 张振国,陈玫,郭玉,等.2007-2008年河北省急性迟缓性麻痹病例脊灰病毒核苷酸变异情况分析[J].预防医学情报杂志,2009,25(12):1020-1022.
[7] Jiang YY, Zhong G, Ban HG, et al. Variation in poliovirus nucleotide in AFP cases in Guangxi[J]. China Tropical Medicine,2011,11(5):550-551. (in Chinese) 蒋玉艳,钟革,班华国,等.广西AFP病例脊髓灰质炎病毒核苷酸变异情况分析[J].中国热带医学,2011,11(5):550-551.
[8] Hou XH, Zhang LB, Leng HY, et al. Discovery of the circulation of typeⅠ vaccine-derived poliovirus in Jiangsu province[J]. Chinese Journal of Vaccines and Immunization,2001,7(6):311-314. (in Chinese) 侯晓辉,张礼璧,冷红英,等.在江苏省发现曾有Ⅰ型脊髓灰质炎疫苗衍生病毒在自然界循环[J].中国计划免疫,2001,7(6):311-314.
[9] An JJ, Zhu H, Yan DM, et al. Genetic characteristics of poliovirus typeⅠin China,2009[J]. China Journal of Vaccines and Immunization,2010,16(2):115-121.(in Chinese) 安军静,朱晖,严冬梅,等.中国2009年Ⅰ型脊髓灰质炎病毒基因特征分析[J].中国疫苗和免疫,2010,16(2):115-121.
[10] Dai ZW, Liu DQ. Poliovirus vaccine strains and vaccine-derived strains of epidemiological significance and Countermeasures[J]. Anhui Journal of Preventive Medicine,2003,9(4):261-263. (in Chinese) 戴振威,刘丹青.脊髓灰质炎病毒疫苗株与疫苗衍生株的流行病学意义及对策[J].安徽预防医学杂志,2003,9(4):261-263.
[11] Zhang LB,Hou XH, Zhu H, et al. The circulation and pathogenesis of type 2 recombinant polioviruses in China[J].Chinese Journal of Vaccines and Immunization,2001,7 ( 3 ) :125-128.( in Chinese) 张礼璧,侯晓辉,朱晖,等. 脊髓灰质炎疫苗重组株病毒在我国的循环及其致病性[J]. 中国计划免疫,2001,7(3):125-128.
[12] WHO. Polio laboratory manuaal. 4th ed. Geneva 27, Switzerland,2002.http://www.who.int/vaccines/en/poliolab/webhelp/Chapter_01/1_4_Transmission_of_polio_virus.htm.
[13] Yan YW. Circulating of vaccine derived poliovirus[J]. Foreign Medical Sciences: Section of Biologics for Prophylaxis, Diagnosis and Therapy,2004,27(5):196-200. (in Chinese) 严有望.脊髓灰质炎疫苗衍生病毒循环的现状[J].国外医学:预防、诊断、治疗用生物制品分册,2004,27(5):196-200.
[14] Fang G, Fu QP, Qi Q, et al. Epidemiological investigation and analysis on AFP cases induced by vaccine-recombinant polioviruses[J]. Chinese Journal of Vaccines and Immunization,2004,10(1):1-3. (in Chinese) 方刚,付清培,漆琪,等.疫苗重组脊髓灰质炎病毒引起的聚集性急性弛缓性麻痹病例流行病学调查与分析[J].中国计划免疫,2004,10(1):1-3.
[15] Li L, Xu AQ, Li RP, et al.Review of the relative studies on vaccine-derived poliovirus[J]. Chinese Journal of Vaccines and Immunization,2007,13(6):595-599. (in Chinese) 李黎,徐爱强,李仁鹏,等.疫苗衍生脊髓灰质炎病毒相关研究进展[J].中国计划免疫,2007,13(6):595-599.
[2] WHO. Circulating vaccine-derived poliovirus1 (cVDPV) 2000-2013. http://www.polio eradication.org/ Data and monitoring/Polio this week/Circulating vaccine derived poliovirus.aspx.
[3] Zhu SL, Zhang Y, Yan DM, et al. Running status and evaluation of Chinese polio laboratories network in 2009 [J]. Chinese Journal of Vaccines and Immunization,2013,19 (3):204-209. (in Chinese) 祝双利,张勇,严冬梅,等.中国2009年脊髓灰质炎实验室网络的运转情况与评价[J].中国疫苗和免疫,2013,19(3):204-209.
[4] Liu DQ, Zhao YP, Chen XQ, et al. Surveillance and epidemiology of cases caused by vaccine derived poliovirus in Anhui province[J]. China Journal of Vaccines and Immunization,2004,10(6):333-335. (in Chinese) 刘丹青,赵月萍,陈晓琴,等.安徽省疫苗变异脊髓灰质炎病毒病例的监测及其流行病学分析[J].中国计划免疫,2004,10(6):333-335.
[5] Zhang H, Xu XY, Chen YW, et al. A case caused by vaccine derived poliovirus typeⅡ[J]. Preventive Medicine Tribune,2007,13(6):2,485. (in Chinese) 张宏,许旭艳,陈杨伟,等.1例Ⅱ型脊髓灰质炎病毒疫苗变异株病例[J].预防医学论坛,2007,13(6):封2,485.
[6] Zhang ZG, Chen M, Guo Y, et al. Variation in poliovirus nucleotide in AFP cases in Hebei province,2007-2008[J]. Journal of Preventive Medicine Information,2009,25 (12) :1020-1022. (in Chinese) 张振国,陈玫,郭玉,等.2007-2008年河北省急性迟缓性麻痹病例脊灰病毒核苷酸变异情况分析[J].预防医学情报杂志,2009,25(12):1020-1022.
[7] Jiang YY, Zhong G, Ban HG, et al. Variation in poliovirus nucleotide in AFP cases in Guangxi[J]. China Tropical Medicine,2011,11(5):550-551. (in Chinese) 蒋玉艳,钟革,班华国,等.广西AFP病例脊髓灰质炎病毒核苷酸变异情况分析[J].中国热带医学,2011,11(5):550-551.
[8] Hou XH, Zhang LB, Leng HY, et al. Discovery of the circulation of typeⅠ vaccine-derived poliovirus in Jiangsu province[J]. Chinese Journal of Vaccines and Immunization,2001,7(6):311-314. (in Chinese) 侯晓辉,张礼璧,冷红英,等.在江苏省发现曾有Ⅰ型脊髓灰质炎疫苗衍生病毒在自然界循环[J].中国计划免疫,2001,7(6):311-314.
[9] An JJ, Zhu H, Yan DM, et al. Genetic characteristics of poliovirus typeⅠin China,2009[J]. China Journal of Vaccines and Immunization,2010,16(2):115-121.(in Chinese) 安军静,朱晖,严冬梅,等.中国2009年Ⅰ型脊髓灰质炎病毒基因特征分析[J].中国疫苗和免疫,2010,16(2):115-121.
[10] Dai ZW, Liu DQ. Poliovirus vaccine strains and vaccine-derived strains of epidemiological significance and Countermeasures[J]. Anhui Journal of Preventive Medicine,2003,9(4):261-263. (in Chinese) 戴振威,刘丹青.脊髓灰质炎病毒疫苗株与疫苗衍生株的流行病学意义及对策[J].安徽预防医学杂志,2003,9(4):261-263.
[11] Zhang LB,Hou XH, Zhu H, et al. The circulation and pathogenesis of type 2 recombinant polioviruses in China[J].Chinese Journal of Vaccines and Immunization,2001,7 ( 3 ) :125-128.( in Chinese) 张礼璧,侯晓辉,朱晖,等. 脊髓灰质炎疫苗重组株病毒在我国的循环及其致病性[J]. 中国计划免疫,2001,7(3):125-128.
[12] WHO. Polio laboratory manuaal. 4th ed. Geneva 27, Switzerland,2002.http://www.who.int/vaccines/en/poliolab/webhelp/Chapter_01/1_4_Transmission_of_polio_virus.htm.
[13] Yan YW. Circulating of vaccine derived poliovirus[J]. Foreign Medical Sciences: Section of Biologics for Prophylaxis, Diagnosis and Therapy,2004,27(5):196-200. (in Chinese) 严有望.脊髓灰质炎疫苗衍生病毒循环的现状[J].国外医学:预防、诊断、治疗用生物制品分册,2004,27(5):196-200.
[14] Fang G, Fu QP, Qi Q, et al. Epidemiological investigation and analysis on AFP cases induced by vaccine-recombinant polioviruses[J]. Chinese Journal of Vaccines and Immunization,2004,10(1):1-3. (in Chinese) 方刚,付清培,漆琪,等.疫苗重组脊髓灰质炎病毒引起的聚集性急性弛缓性麻痹病例流行病学调查与分析[J].中国计划免疫,2004,10(1):1-3.
[15] Li L, Xu AQ, Li RP, et al.Review of the relative studies on vaccine-derived poliovirus[J]. Chinese Journal of Vaccines and Immunization,2007,13(6):595-599. (in Chinese) 李黎,徐爱强,李仁鹏,等.疫苗衍生脊髓灰质炎病毒相关研究进展[J].中国计划免疫,2007,13(6):595-599.
|
扩展功能
|
|
| 本文信息 | |
| PDF全文 | |
| HTML全文 | |
| 参考文献 | |
| 服务与反馈 | |
| 加入引用管理器 | |
| 引用本文 | |
| Email Alert | |
| 本文作者相关文章 | |
| 杨北方 | |
| 李书华 | |
| 刘娜 | |
| 舒端 | |
| 邓振刚 | |
| PubMed | |
| Article by YANG Bei-fang | |
| Article by LI Shu-hua | |
| Article by LIU Na | |
| Article by SHU Duan | |
| Article by DENG Zhen-gang | |