扩展功能
文章信息
- 文艳苹, 于新芬, 周银燕, 寇宇, 郑伟, 郑之北
- WEN Yan-ping, YU Xin-fen, ZHOU Yin-yan, KOU Yu, ZHENG Wei, ZHENG Zhi-bei
- 杭州市急性呼吸道感染儿童中WU多瘤病毒感染的流行病学及基因特征分析
- Epidemiology of WU polyomavirus infection in children with acute respiratory disease and the virus genetic characteristics in Hangzhou
- 疾病监测, 2015, 30(2): 103-107
- Disease Surveillance, 2015, 30(2): 103-107
- 10.3784/j.issn.1003-9961.2015.02.006
-
文章历史
- 收稿日期:2014-11-06
急性呼吸道感染是造成5岁以下儿童死亡的主要疾病。研究发现90%以上的急性呼吸道感染是由病毒引起。尽管近年来对呼吸道病毒感染的病原学已有较深入的研究,但目前仍有10%~39%的急性呼吸道感染病因不明。
WU多瘤病毒(WU polyomavirus,WUPyV)是2007年由Gaynor等[1]在肺炎患者呼吸道标本中检测到的新病毒。自美国和澳大利亚检出WUPyV后,法国、德国、加拿大、韩国、泰国等多个国家相继检出该病毒[2,3,4,5],并对各国的WUPyV进行了研究。研究发现,WUPyV阳性患者多表现有细支气管炎、哮喘、肺炎等呼吸道疾病症状,表明WUPyV与呼吸道感染有关。由于尚无适合WUPyV培养的细胞株和动物模型,导致WUPyV病原学研究相对滞后。
我国北京、天津、福建、汕头、兰州等地区也开展了WUPyV的筛查工作[6,7,8,9,10]。其中天津地区急性呼吸道感染患儿的WUPyV检出率为16.1%,是国内已报道的最高检出率。
浙江省仅温岭、湖州两地开展了WUPyV研究工作[11,12]。WUPyV在杭州市婴幼儿中流行情况尚不清楚,本次研究旨在调查杭州市急性呼吸道感染儿童中WUPyV流行情况,阐明该病毒的流行特征、基因型别和基因组结构特点,为评估该病毒的危害性,确定今后的病毒筛查范围提供依据。
1 材料与方法 1.1 标本来源采集2011年3月至2013年6月间至浙江省儿童医院就诊并住院的急性呼吸道感染儿童的鼻咽吸取物标本,并记录患儿的临床特征和人口学特征。在采集的鼻咽吸取物标本中加入3 ml DEME采样液,冰瓶中带到实验室进行基因组DNA抽提。
1.2 WUPyV鉴定采用病毒RNA/DNA提取试剂盒(QIAGEN RNA/DNA Mini Kit DNA,QIAGEN)抽提鼻咽吸取物的基因组DNA,分装后放-20 ℃保存待用。DNA抽提具体步骤参考产品说明书。以WUPyV的VP2编码基因片段作为筛查靶点,采用文献报道的引物AG0044、AG0045进行聚合酶链反应(polymerase chain reaction,PCR),扩增条件与Gaynor等[1]报道一致。PCR扩增以携带WUPyV基因片段的AP-p002质粒(购自addgene网站)作为阳性对照。PCR扩增结束后,采用2%琼脂糖凝胶电泳检测,阳性产物片段大小为250 bp。符合片段大小的PCR产物经Qiagen公司的QIAquickGel Extraction试剂盒纯化后,送上海生物工程公司进行测序。
1.3 WUPyV基因分型以WUPyV阳性样本的基因组为模板,VP2/1中间序列(1620~2299 bp)为基因分型位点,采用引物WUT-F和WUT-R进行PCR扩增 [13],扩增条件为:95 ℃ 5 min;94 ℃ 30 s,55 ℃ 30 s,72 ℃ 45 s,循环35次;72 ℃ 10 min。PCR扩增以AP-p002质粒作为阳性对照,扩增产物经Qiagen公司的QIAquickGel Extraction试剂盒纯化后,送上海生物工程公司进行测序。将VP2/1中间序列递交至GenBank,序列号为KM265133~KM265136和KM361627~KM361632。
1.4 WUPyV全基因组扩增及测序根据基因分型结果,选取代表性毒株进行PCR扩增及测序。PCR扩增所用引物如表 1所示。扩增条件为:95 ℃ 5 min;94 ℃ 30 s,55 ℃ 30 s,72 ℃ 45 s(WU-Seq10F、WU-Seq10R引物对)或2 min(表 1中其他引物对),循环35次;72 ℃ 10 min。PCR扩增以携带WUPyV基因片段的AP-p002和AP-p003质粒(购自addgene网站)作为阳性对照。扩增产物经Qiagen公司的QIAquickGel Extraction试剂盒纯化后,送上海生物工程公司进行测序。递交至GenBank,序列号为KM265136。
| 引物 | 位点 | 序列(5′~3′) | 产物(bp) |
| WU 1-F | 1-19 | GCC GCA GTC CTC CTT ATT A | 1336 |
| WU 1-R | 1336-1316 | GTA ACC GTT CTC GTT GTC TTC | |
| Wu 2-F | 1114-1135 | GAC GTG TTC AAG AGA ATT GCC TAT G | 1410 |
| Wu 2-R | 2523-2499 | AAA AAT CTG GAA AGC CCT GTA TGT A | |
| WU 3-F | 2088-2106 | GGG GTG TAG GAG GTA TTG C | 1322 |
| WU 3-R | 3409-3391 | AAC TGT TGC TGC TGC TTT A | |
| WU 4-F | 3079-3098 | TTT ATG AAA TCT AGG AGC CA | 2096 |
| WU 4-R | 5174-5156 | AGG CTA AAG AAG GCA AAA T | |
| WU-Seq10F | 4824-4848 | CTT CAA AAA CAT CAC CAT AAA CTT | 658 |
| WU-Seq10R | 252-231 | AAG GGC ACC AGT ATT GTA TTC C |
采用BioEdit 9.7软件对基因组序列进行拼接。采用Clustal 1.81软件进行序列比对[14],Mega 4.0软件构建进化树,构建采用邻接法,Bootstrap重复值设为1000。基因组重组分析采用软件RDP4和Splits Tree4’s[15,16],选择压力分析选用PAML 4软件。
1.6 其他呼吸道病毒的检测使用PCR或反转录-聚合酶链反应(reverse transcription-polymerase chain reaction,RT-PCR)筛查WUPyV阳性标本中其他呼吸道病毒的合并感染情况,方法同Zhuang等[9]的报道。检测的病毒包括呼吸道合胞病毒(respiratory syncytial virus,RSV)、人博卡病毒(human bocavirus,HBoV)、腺病毒(adenovirus,ADV)、鼻病毒(human rhinovirus,RhV)、流感病毒A、B型(influenza virus A and B,FluA、FluB)、副流感病毒1、2、3型(parainfluenza virus types 1,2 and 3,PIV1、PIV2、PIV3)、人偏肺病毒(human metapneumovirus,hMPV)等10种(型)病毒。
1.7 统计学处理采用
2011年3月至2013年6月共采集急性呼吸道感染儿童的鼻咽吸取物标本722份,以其基因组DNA为模板,VP2编码基因为筛选靶点,进行普通PCR扩增。经电泳检测发现,10份样本的PCR扩增产物的大小与阳性扩增结果相符,约250 bp。对这10份样本的PCR扩增产物进行测序,发现扩增产物大小为250 bp,序列间相似性为100%,与WUPyV病毒株B8805 VP2编码区(1331~1580 bp)的相似性为100%。以上结果表明这10份样本均为WUPyV阳性,WUPyV检出率为1.4%(10/722)。
2.2 WUPyV流行特征10例WUPyV阳性病例中,3例源自2011年,5例源自2012年,2例源自2013年。WUPyV感染主要发生在夏季、秋季和冬季。男性9例(90%),女性1例(10%),男女比例为9 ∶ 1,与采样人群的男女比例(1.8 ∶ 1)相比,差异无统计学意义(
| 病例 | 年龄(月龄) | 性别 | 检出时间(年-月) | 合并感染(1) | 发热 | 咳嗽 | 气喘 | 临床诊断 |
| 注:(1)HBoV:人博卡病毒; RSV:呼吸道合胞病毒; FluB:流感病毒B型; RHV:鼻病毒; hMPV:人偏肺病毒。 | ||||||||
| 1 | 10 | 男 | 2011-06 | HBoV | + | + | + | 支气管肺炎 |
| 2 | 5 | 男 | 2011-08 | + | + | + | 肺炎 | |
| 3 | 12 | 男 | 2011-10 | RSV | + | + | + | 支气管肺炎 |
| 4 | 27 | 男 | 2012-01 | RSV,FluB | + | + | + | 肺炎 |
| 5 | 48 | 男 | 2012-07 | + | + | + | 支气管肺炎 | |
| 6 | 12 | 女 | 2012-08 | + | + | + | 喉炎 | |
| 7 | 6 | 男 | 2012-09 | - | + | + | 喉炎 | |
| 8 | 5 | 男 | 2012-12 | + | + | - | 支气管肺炎 | |
| 9 | 7 | 男 | 2013-01 | RSV | - | + | - | 肺炎 |
| 10 | 4 | 男 | 2013-05 | RHV,hMPV,FluB | + | + | - | 细支气管炎 |
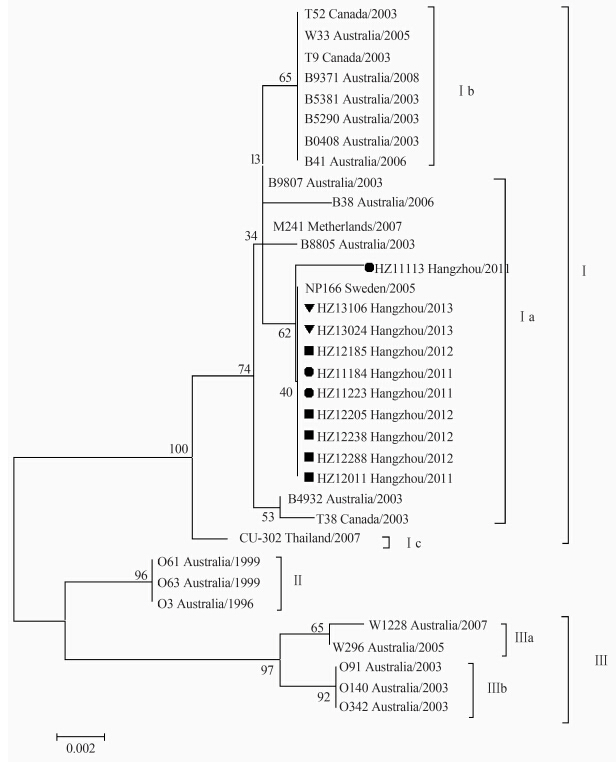
以VP2/1中间序列作为分型位点,进行PCR扩增。扩增产物测序完成后,构建系统发生树。测序结果表明,VP2/1中间序列长度为679 bp。10例WUPyV病例中 ,共有2类VP2/1中间序列。其中2011年检出的1株病毒株(HZ11113)为一种类型,另外9株病毒株与毒株HZ11113相差2个碱基,序列间同源性为99.71%~100%。 基于VP2/1中间序列构建系统发生树,结果如图 1所示。系统发生树共包括3个大簇(Bootstrap值>95%),分别对应基因型Ⅰ、Ⅱ和Ⅲ,与Bialasiewicz等 [13]的分型结果一致。基因型Ⅰ分为Ⅰa、Ⅰb、Ⅰc三个亚簇,基因型Ⅲ分为Ⅲa和Ⅲb两个亚簇。杭州地区的WUPyV病毒株与WUPyV NP166聚集成簇,继而落在Ⅰa域中。而WUPyV NP166是2005年分离自瑞典一份鼻咽吸取物标本。以上结果表明2011 2013年间杭州地区急性呼吸道感染儿童中流行的WUPyV的基因型为Ⅰa型。
|
| 图 1 基于VP2/1中间序列(679 bp)构建的系统发生树 Figure 1 Phylogenetic tree based on VP2/1 interface typing region (679 bp) of WUPyV strains 注:●2011年杭州检出株;■2012年杭州检出株;▼2013年杭州检出株。 |
根据VP2/1中间序列特征,挑选具有代表性的WUPyV病毒株HZ13024进行基因组测序。HZ13024基因组大小为5229 bp,与GenBank中WUPyV基因组序列相似性为99.8%~99.9%。全基因组含有5个编码序列(CDS),包括位于一条链上的LTAg和STAg抗原早期编码区,及位于另一条链上的衣壳蛋白VP1、VP2、VP3的晚期编码区。对WUPyV进行选择压力和重组分析,显示WUPyV基因组未发生重组事件(
本研究共收集急性呼吸道感染儿童鼻咽吸取物标本722份,10份为WUPyV阳性,检出率为1.4%。与我国北京、兰州、天津、汕头等地相比(分别为5.6%、2.2%、16.1%和2.0%)[6,7,8,9],杭州地区检出率较低。总体上,中国WUPyV检出率低于韩国和日本[3,17],与法国、德国、美国、加拿大等地相当[2,4,5,18]。杭州WUPyV感染主要发生在夏季、秋季和冬季,与中国其他城市相比稍有差异:兰州WUPyV感染高发期为秋冬季,天津WUPyV无感染高发季,全年均可流行,可能与不同地域气候差异有关。杭州WUPyV阳性病例年龄均小于48月龄。血清学研究表明[4,19],人群中WUPyV感染率高达43.1%~49.4%,主要发生在幼儿期,当幼儿免疫力低下时,病毒可再次被激活。此流行病学特征与多瘤病毒BK病毒(BK virus,BKV)和JC病毒(JC virus,JCV)相似。
杭州流行的WUPyV基因型别为Ⅰa型。结合本次研究以及其他地区WUPyV的基因分型结果发现[6],基因型别Ⅰa是中国WUPyV主要流行型别。与之前WUPyV基因型别与样本地理来源相关的研究结论一致[1]。除基因型别Ⅰa外,基因型别Ⅲb在北京儿童急性呼吸道感染样本中也有检出[6]。在其他多瘤病毒(BKV和JCV)中,基因型别与病毒致病性和疾病严重性密切相关。不同基因型别的WUPyV毒株是否也存在致病性差异,还需要进一步流行病学调查研究。
杭州地区WUPyV毒株HZ13024与GenBank中WUPyV基因组序列相似性为99.8%~99.9%。基因组未发生重组事件,且大多数氨基酸位点主要受净化选择。这些结果表明WUPyV的基因组序列高度保守。在VP1、VP2、VP3、LTAg和STAg五个蛋白编码基因中,衣壳蛋白(VP1、VP2和VP3)编码基因的d(N)/d(S)值高于抗原(LTAg和STAg)编码基因,表明衣壳蛋白编码基因承受的净化选择压力较弱,可能与逃避宿主免疫识别有关。单位点正向选择检测发现,VP2蛋白的287位氨基酸位点为正向选择位点。该位点的变异具有基因型别特异性。Ⅲ型WUPyV的VP2编码基因中,1432位点发生改变(G→C),导致氨基酸Gln→Glu或Asp。由于该位点落在VP2蛋白D1区(318~353aa)、DNA结合区(358~409aa)、核定位信号区(377~384aa)等功能域外,是否会引起细胞嗜性或抗原改变还未知。
本次研究共检测到10例WUPyV感染病例,其中5例仅检测到WUPyV一种病原,表明WUPyV与儿童急性呼吸道感染相关。WUPyV在不同人群(婴幼儿、老年人、免疫力低下人群等)中的致病性、是否与肿瘤相关、除呼吸道外是否具有器官组织趋向性等问题,还有待进一步研究和阐明。
| [1] | Gaynor AM, Nissen MD, Whiley DM, et al. Identification of a novel polyomavirus from patients with acute respiratory tract infections[J]. PLoS Pathog,2007,3(5):e64. |
| [2] | Abed Y, Wang D, Boivin G. WU polyomavirus in children, Canada[J]. Emerg Infect Dis,2007,13(12):1939-1941. |
| [3] | Han TH, Chung JY, Koo JW, et al. WU polyomavirus in children with acute lower respiratory tract infections, South Korea[J]. Emerg Infect Dis,2007,13(11):1766-1768. |
| [4] | Neske F, Prifert C, Scheiner B, et al. High prevalence of antibodies against polyomavirus WU, polyomavirus KI, and human bocavirus in German blood donors[J]. BMC Infect Dis,2010,10:215. |
| [5] | Foulongne V, Brieu N, Jeziorski E, et al. KI and WU polyomaviruses in children, France[J]. Emerg Infect Dis,2008,14(3):523-525. |
| [6] | Zhao L, Qian Y, Zhu R, et al. Identification of WU polyomavirus from pediatric patients with acute respiratory infections in Beijing, China[J]. Arch Virol,2010,155(2):181-186. |
| [7] | Li XY, Chen JY, Kong M, et al. Role of WU polyomavirus in children with acute respiratory tract infections[J]. Journal of Pathogen Biology,2011,6(1):1-4. (in Chinese) 李晓燕,陈锦英,孔梅,等. WU多瘤病毒在儿童急性呼吸道感染中的作用[J]. 中国病原生物学杂志,2011,6(1):1-4. |
| [8] | Yuan XH, Xu ZQ, Xie ZP, et al. WU polyomavirus and KI polyomavirus detected in specimens from children with acute respiratory tract infection in China[J]. Chinese Journal of Clinical and Experimental Pathology,2008,22(1):21-23. (in Chinese) 原新慧,徐子乾,谢志萍,等. 我国急性呼吸道感染患儿中检测到KI和WU多瘤病毒[J]. 中华实验和临床病毒学杂志,2008,22(1):21-23. |
| [9] | Zhuang WL, Lu XD, Lin GY, et al. WU polyomavirus infection among children in South China[J]. J Med Virol,2011,83(8):1440-1445. |
| [10] | Xiu WQ, Shen XN, Liu GH, et al. Sequencing and analysis of the complete genome sequence of WU polyomavirus in Fuzhou, China[J]. Chinese Journal of Virology,2011,27(2):165-169. (in Chinese) 修文琼,沈晓娜,刘光华,等. 2株WU多瘤病毒全基因组序列测定和分析[J]. 病毒学报,2011,27(2):165-169. |
| [11] | Lin F, Zheng MY, Li H, et al. Discovery and identification of WU polyomavirus in children from Zhejiang region[J]. Chinese Journal of Virology,2008,24(1):69-71. (in Chinese) 林峰,郑美云,李桦,等. WU多瘤病毒在中国浙江地区的发现与鉴定[J]. 病毒学报,2008,24(1):69-71. |
| [12] | Song JF, Xing JM. WU polyomavirus detected by real-time PCR[J]. Chinese Journal of Nosocomiology,2009,19(10):1317-1320. (in Chinese) 宋娟芳,邢建明. WU多瘤病毒实时荧光聚合酶链检测方法的建立与应用[J]. 中华医院感染学杂志,2009,19(10):1317-1320. |
| [13] | Bialasiewicz S, Rockett R, Whiley DW, et al. Whole-genome characterization and genotyping of global WU polyomavirus strains[J]. J Virol,2010,84(12):6229-6234. |
| [14] | Thompson JD, Gibson TJ, Plewniak F, et al. The CLUSTAL_X windows interface: flexible strategies for multiple sequence alignment aided by quality analysis tools[J]. Nucleic Acids Res,1997,25(24):4876-4882. |
| [15] | Martin DP, Williamson C, and Posada D. RDP2: recombination detection and analysis from sequence alignments[J]. Bioinformatics,2005,21(2):260-262. |
| [16] | Huson DH, Bryant D. Application of phylogenetic networks in evolutionary studies[J]. Mol Biol Evol,2006,23(2):254-267. |
| [17] | Okada M, Hamada H, Sato-Maru H, et al. WU polyomavirus detected in respiratory tract specimens from young children in Japan[J]. Pediatr Int,2013,55(4):536-537. |
| [18] | Le BM, Demertzis LM, Wu G, et al. Clinical and epidemiologic characterization of WU polyomavirus infection, St. Louis, Missouri[J]. Emerg Infect Dis,2007,13(12):1936-1938. |
| [19] | Miller MA, Weibel C, Kahn JS, et al. Seroepidemiology of WU polyomavirus among children exposed perinatally to HIV-1[J]. J Med Virol,2012,84(2):188-193. |
 2015, Vol. 30
2015, Vol. 30


