扩展功能
文章信息
- 刘思超, 罗泽燕, 徐励琴, 杨剑英, 冯伟明, 邬军军
- LIU Si-chao, LUO Ze-yan, XU Li-qin, YANG Jian-ying, FENG Wei-ming, WU Jun-jun
- 广东省惠州市集中空调系统冷却水及冷凝水中嗜肺军团菌脉冲场凝胶电泳分型分析
- Pulsed field gel electrophoresis typing of Legionella pneumophila in cooling water and condensed water from centralized air conditioning system in Huizhou
- 疾病监测, 2017, 32(5): 382-386
- Disease Surveillance, 2017, 32(5): 382-386
- 10.3784/j.issn.1003-9961.2017.05.008
-
文章历史
- 收稿日期:2016-12-21
嗜肺军团菌(Legionella pneumophila,LP)是一种革兰阴性兼性细胞内致病菌,广泛存在于各种水环境中,在空调系统、冷却塔和供水系统中尤为常见,是引起军团菌病的主要病原体[3-4]。自军团菌被发现以来,国内外相继报道多起军团菌病暴发流行及散发病例[5-6]。该病病死率高,是世界各国普遍关注的公共卫生问题[2,7]。军团菌病主要通过气溶胶的方式进行传播。有关报道证实,空调冷却塔是军团病暴发的重要传染源[8-10]。目前应用于军团菌分型研究的分子分型方法较多,如脉冲场凝胶电泳(pulsed-field gel electrophoresis,PFGE)、多位点基因分型(sequence-based typing,SBT)、多位点可变数目串联重复序列多态性(multiple locus variable number tandem repeat analysis,MLVA)等,其中PFGE在细菌分型的实际应用中显示了很好的分辨力和流行病学调查能力[8]。为了解惠州市嗜肺军团菌分子特征,本研究采用PFGE对惠州市公共场所集中空调冷却水及冷凝水中分离到的嗜肺军团菌进行基因分型,现将结果报告如下。
1 材料与方法 1.1 材料 1.1.1 菌株35株嗜肺军团菌为2012-2016年惠州市公共场所集中空调系统冷却水及冷凝水中分离获得,并经生化鉴定、血清学凝集试验鉴定为Lp1型或Lp2~14型。2012年14株,2013年3株,2014年6株,2015年10株及2016年2株。菌株来源于5类不同的场所,见表 1。菌株地区分布为惠城区江北、南坛下埔、麦地河南岸等片区26株和仲恺高新区9株。35株菌来自34个集中空调系统。PFGE实验分子质量标准对照的布伦敦卢普沙门菌(Salmonella braenderup)H9812菌株,由广东省疾病预防控制中心(CDC)病原微生物所提供。
| 来源场所 | 株数 | 冷却水 | 冷凝水 | |||
| Lp1型 | Lp2~14型 | Lp1型 | Lp2~14型 | |||
| 酒店 | 5 | 1 | 3 | 1 | 0 | |
| 商场 | 10 | 3 | 6 | 0 | 1 | |
| 超市 | 7 | 2 | 4 | 0 | 1 | |
| 写字楼 | 11 | 7 | 4 | 0 | 0 | |
| 娱乐场所 | 2 | 2 | 0 | 0 | 0 | |
| 合计 | 35 | 15 | 17 | 1 | 2 | |
军团菌生长平板(buffered charcoal yeast Extract agar plate,BCYE)购自广东环凯生物科技有限公司;军团菌乳胶凝集试剂盒购自英国OXOID公司;XbaⅠ和AscⅠ限制性内切酶购自英国NEB公司;蛋白酶K购自德国MERCK公司;SeaKem Gold Agarose购自瑞士Lonza公司;Tris-HCl和EDTA等试剂购自北京Solarbio公司。均在有效期内使用。
1.1.3 主要仪器脉冲场凝胶电泳仪(Bio-Rad CHEF Mapper),凝胶成像仪(Bio-Rad GEL Doc 2000),菌液比浊仪(BioMerieux Vitek colorimeter),CO2恒温培养箱(Precision),恒温水浴箱(Grant),水浴摇床(Grant),双重振荡摇床(Thermo Fisher)等。
1.2 方法 1.2.1 PFGE该方法由中国CDC传染病预防控制所呼吸道传染病室提供,采用军团PFGE分型首选内切酶AscⅠ[11] (10 000 U/ml)对细菌基因组进行酶切。
1.2.1.1 胶块的制备接种军团菌菌株于含L-半胱氨酸的BCYE平板上,在CO2培养箱37 ℃培养48 h。用棉签刮取适量细菌,均匀悬浊于细菌悬浊液(CSB)中,调节菌悬液浓度为3.8~4.2个麦氏单位(MCF)。取400 μl细菌悬浊液于1.5 ml离心管中,加入20 μl蛋白酶K(20 mg/ml),再与400 μl的1% SeaKem Gold Agarose : 1%(SDS)混合均匀,将混合物加入模具,室温下凝固。
1.2.1.2 细胞的裂解胶块凝固后,放入5 ml含有25 μl蛋白酶K(20 mg/ml)的细胞裂解液(CLB)中,54 ℃摇床中孵育2 h,转速150~170 r/min。然后用50 ℃ 15 ml灭菌蒸馏水洗胶块2次;再用50 ℃ 15 ml TE洗胶块4次,每次10~15 min。
1.2.1.3 酶切用约2 mm宽的胶块放入1.5 ml离心管中,加入200 μl预酶切缓冲液于37 ℃孵育10 min,吸出预酶切缓冲液,加入200 μl AscⅠ酶切液于37 ℃酶切4 h。
1.2.1.4 电泳将酶切后的胶块贴于梳齿包埋于1% SeaKem Gold Agarose,待胶凝固后,将胶小心放入盛有2 L 0.5×TBE缓冲液的电泳槽中,电泳19 h,电泳起始转换时间6.8 s,终止转换时间54.2 s,电压为6 V/cm,电场夹角120°,初始电流控制在135 mA左右,温度14 ℃。
1.2.1.5 图像的获取电泳结束后用400 ml EB溶液(1 μg/ml)染色30 min,再用纯水脱色60~90 min(每20 min换一次纯水),用Gel Doc 2000拍摄图像。
1.2.2 聚类分析将实验菌株全染色体DNA酶切图谱导入BioNumerics(version 6.6,Applied Maths.Inc)软件,识别图谱条带,经统一的分子质量标准对照沙门菌H9812进行校准,标定条带位置,必要时进行手工校正。图谱之间的相似性系数用距离法(Dice系数,dice coefficients,SD)计算。根据图谱之间的相似性系数,用非加权配对算术平均法(unweighted pair groupaverage method,UPGMA)进行聚类,并构建聚类树。
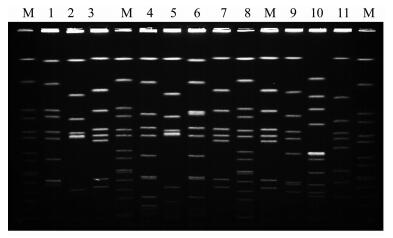
2 结果 2.1 嗜肺军团菌PFGE35株嗜肺军团菌经AscⅠ酶切电泳后,DNA片段得到良好分离,不同的菌株分子质量在20 ~1 200 kb之间,DNA条带数目为7~13条之间。部分电泳结果见图 1。
|
| 图 1 部分实验菌株PFGE图谱 Figure 1 PFGE pattern of part test strains 注:M:分子质量标准Marker(H9812);1~11:实验菌株。 |
| |
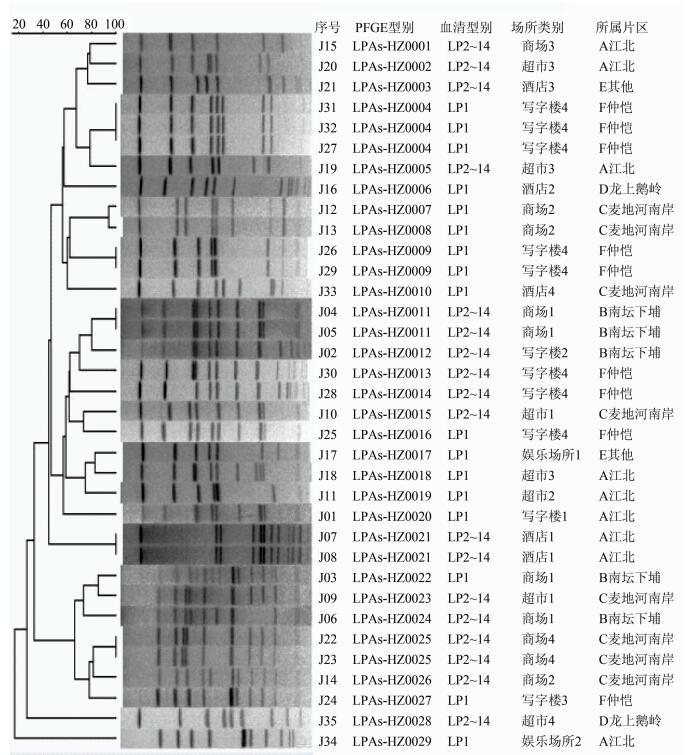
35株嗜肺军团菌全染色体DNA酶切图谱经BioNumerics 6.6软件进行聚类分析,共分为29种PFGE型,按照PulseNet China的带型命名原则,分别命名为LPAs.HZ0001~LPAs.HZ0029,菌株间相似系数在21.70%~100.00%之间,每种带型包含1~3株菌,存在5组带型一样的菌株,不存在优势型别,见图 2。
|
| 图 2 35株嗜肺军团菌PFGE结果聚类树 Figure 2 Cluster analysis of 35 strains of L. pneumophila by PFGE |
| |
本研究的35株嗜肺军团菌,分别来自惠城区江北、南坛下埔、麦地河南岸等片区和仲恺高新区,菌株全染色体DNA酶切图谱经聚类分析,各地区菌株间相似性系数在21.70% ~100.00%之间,见表 2。
| 地区(片区) | 株数 | 菌株编号 | 各地区菌株间相似性系数(%) |
| 惠城区 | |||
| A江北 | 9 | J01、J07、J08、J11、J15、J18、J19、J20、J34 | 21.70~100.00 |
| B南坛下埔 | 5 | J02、J03、J04、J05、J06 | 32.00~100.00 |
| C麦地河南岸 | 8 | J09、J10、J12、J13、J14、J22、J23、J33 | 41.90~100.00 |
| D龙上鹅岭 | 2 | J16、J35 | 32.40 |
| E其他 | 2 | J17、J21 | 57.30 |
| 仲恺区 | |||
| F高新区 | 9 | J24、J25、J26、J27、J28、J29、J30、J31、J32 | 28.60~100.00 |
各组PFGE型别相同的菌株均来源于同一场所。例如,同属于LPAs.HZ0004型别的J27、J31和J32,均来源于仲恺区F高新区的写字楼4。部分同一场所来源的菌株均属于相同的PFGE型。来源于惠城区A片区酒店1的J07和J08,均属LPAs.HZ0021型别。也有部分同一场所来源的菌株存在2种以上PFGE型别,来源于惠城区A片区超市3的菌株J18、J19、J20分别属于3个PFGE型别(LPAs.HZ0018、LPAs.HZ0005、LPAs.HZ0002),型别间相似性系数差异较大,菌株间亲缘关系较远,无优势株。部分场所存在冷却水和冷凝水中分离的嗜肺军团菌PFGE型别相同的现象。J22、23是分别于惠城区C片区商场4的冷却水和冷凝水中分离的菌株,PFGE型别相同(LPAs.HZ0025)。
2.5 LP1血清型嗜肺军团菌菌株PFGE分型35株嗜肺军团菌中,经血清学凝集试验鉴定为LP1型的嗜肺军团菌菌株有16株,可分为13种PFGE型别,菌株间相似性系数为21.70%~100.00%;而Lp2~14型因条件所限未进行单一血清型分型。
3 讨论据相关报道,超过90%的军团菌病暴发由嗜肺军团菌引起[3]。嗜肺军团菌有15个血清型,其中嗜肺军团菌1型(Lp1) 为主要的致病血清型[2]。传统的血清分型方法分辨力低,难以进行疫情暴发的溯源。PFGE因其重复性好、分辨力强、易于标准化的特点,被誉为细菌分子分型技术的“金标准”[12],已成为细菌传染性疾病的暴发流行调查及传染源溯源的重要手段[13]。
随着城市的经济发展,大型集中空调设备逐渐普及到各类公共场所中,客观上为嗜肺军团菌的滋生提供了理想场所,存在感染人群引起疾病的可能。因此,在分子水平对环境嗜肺军团菌进行监测,掌握该地区嗜肺军团菌的菌株基因特性,有着非常重要的意义。目前惠州市CDC对公共场所的监测工作范围集中在惠城和仲恺两大城区,监测的场所类别包括酒店、商场、超市、写字楼和娱乐场所。如发生军团菌病暴发或流行,可以借助PFGE作为暴发调查工具溯源,明确传染源和传播途径,也可将引起暴发的嗜肺军团菌与惠州地区已有菌型进行比对,以便对疫情的暴发和流行提前做出预警,针对性地对特定地区或类别的场所实施环境消毒和人群防护,为公共卫生干预提供数据支持。
本实验结果显示,嗜肺军团菌PFGE带型多态性大,无优势型别,提示菌株间基因多态性大,可能存在多个克隆系,与其他城市的报道结果一致[7,14-15]。有报道,部分城市不同地区中央空调冷却塔水之间存在军团菌交叉污染的可能性[14-15],而惠州市不同地区菌株PFGE型别差异明显,菌株间相似性系数在21.70%~100.00%之间,未见相同PFGE型别的嗜肺军团菌,未发现本地区集中空调系统间存在嗜肺军团菌的交叉污染现象。同一地区,嗜肺军团菌酶切图谱呈现多样性,菌株间相似性系数存在差异,充分体现了嗜肺军团菌基因多态性。从相同场所分离的菌株存在多种型别,表明同一水系中可以多个克隆系的嗜肺军团菌共存。部分场所的冷却水和冷凝水中同时检出嗜肺军团菌,且PFGE型别相同,提示集中空调冷却塔水可能已污染系统周边环境,导致风机盘管表面甚至是周围空气中含有同克隆系的嗜肺军团菌,存在较大的感染人群引起疾病的风险。建议加强对集中空调冷却塔定期消毒,并在消毒后进行效果评价,避免军团菌滋生引起军团菌病暴发[9]。
从惠州市近几年公共场所集中空调冷却水及冷凝水的监测结果可见,该市存在较多Lp1型嗜肺军团菌(16/35),该菌型已在世界范围内引起多次军团菌病暴发,提示惠州市公共场所存在潜在的危害,仍需加强对公共场所集中空调冷却水及冷凝水监测工作,以预防军团菌病暴发或流行。此次研究发现,用传统血清学分型方法确认为Lp1型的嗜肺军团菌经PFGE分型后,得到13种不同的图谱,各菌株间存在高度多态性,表明仅凭血清学分型方法无法进行疫情暴发的溯源,而PFGE分型技术可以具体掌握菌株的基因型别,证实了PFGE技术在分子分型和流行病学溯源调查中的重要作用。
本研究将PFGE技术应用于惠州市嗜肺军团菌环境分离株的分子分型,初步建立了该地区嗜肺军团菌PFGE分型数据库,当数据库获得足够数量的流行病学上有关联的嗜肺军团菌,不仅为今后对环境嗜肺军团菌进行分子水平监测提供基础资料,更能为该地区嗜肺军团菌分子流行病学调查提供重要依据。
作者贡献:
刘思超 ORCID:0000-0001-6516-8742
刘思超:负责集中空调系统冷却水及冷凝水中嗜肺军团菌检测及PFGE试验,收集并整理数据,撰写论文及相关材料的准备
罗泽燕:参与集中空调系统冷却水及冷凝水中嗜肺军团菌检测及PFGE试验,参与数据分析讨论
徐励琴:提供实验条件给予支持
杨剑英、冯伟明:实验前期培养基购买、配置及部分耗材准备
邬军军:负责集中空调系统冷却水及冷凝水采样工作
| [1] | Ren HY, Zhu BQ, Zhou HJ, et al. Typing of Legionella pneumophila strains isolated from environmental water systems using pulsed-field gel electrophoresis[J]. Disease Surveillance, 2009, 24(12): 970–973. (in Chinese) 任红宇, 朱兵清, 周海健, 等. 环境水系分离嗜肺军团菌脉冲场凝胶电泳的分型研究[J]. 疾病监测, 2009, 24(12): 970–973. DOI:10.3784/j.issn.1003-9961.2009.12.023 |
| [2] | Yang M, Cheng HJ, Xiong CH, et al. Genetic characteristics of Legionella pneumophila serotype 1 strains[J]. Chinese Journal of Zoonoses, 2010, 26(12): 1151–1153. (in Chinese) 杨梦, 程慧键, 熊长辉, 等. 嗜肺军团菌血清1型基因检测及分子分型研究[J]. 中国人兽共患病学报, 2010, 26(12): 1151–1153. DOI:10.3969/j.issn.1002-2694.2010.12.018 |
| [3] | Guo YM, Zhou JK. Research progress in molecular typing of Legionella pneumophila[J]. J Environ Health, 2010, 27(6): 555–557. (in Chinese) 郭玉梅, 周吉坤. 嗜肺军团菌分子分型研究进展[J]. 环境与健康杂志, 2010, 27(6): 555–557. |
| [4] | Lin YW, Chen SY. Molecular Biology Detection and Epidemiological Typing Method for Legionella pneumophila[J]. Journal of Tropical Medicine, 2009, 9(7): 840–842. (in Chinese) 林云万, 陈守义. 嗜肺军团菌分子生物学检测及流行病学分型方法[J]. 热带医学杂志, 2009, 9(7): 840–842. |
| [5] | Qin T, Xia J, Ren H, et al. Liver cirrhosis as a predisposing condition for Legionnaires disease:a report of four laboratory-confirmed cases from China[J]. J Med Microbiol, 2012, 61(7): 1023. |
| [6] | Lu F, Jin YL, Cheng YB. Epidemiological survey of Legionnaires disease[J]. Foreign Medical Sciences:Section of Hygiene, 2008, 32(2): 78–83. (in Chinese) 路凤, 金银龙, 程义斌. 军团菌病的流行概况[J]. 国外医学卫生学分册, 2008, 32(2): 78–83. |
| [7] | Zhang Z, Zhu SR, Xu BX. Study on gene detection and molecular characteristics of Legionella pneumophila[J]. Chinese Journal of Health Laboratory Technology, 2007, 17(11): 1978–1980. (in Chinese) 张政, 朱水荣, 徐宝祥. 嗜肺军团菌基因检测及分子特征研究[J]. 中国卫生检验杂志, 2007, 17(11): 1978–1980. DOI:10.3969/j.issn.1004-8685.2007.11.022 |
| [8] | Qin T, Ren HY, Zhou HJ. Evaluation of pulsed-field gel electrophoresis for Legionella subtyping[J]. Disease Surveillance, 2011, 26(3): 182–186. (in Chinese) 秦天, 任红宇, 周海健. 脉冲场凝胶电泳用于军团菌分型能力的评价[J]. 疾病监测, 2011, 26(3): 182–186. |
| [9] | Han H, Zuo F, Wu HL. Legionella isolation from cooling tower water collected in Tianjin airport and the evaluation of disinfection measures[J]. Chinese Frontier Health Quarantine, 2016, 39(1): 33–35. (in Chinese) 韩辉, 左锋, 吴海磊. 天津空港口岸中央空调冷却塔水检出军团菌以及消毒处理效果评价[J]. 中国国境卫生检疫杂志, 2016, 39(1): 33–35. |
| [10] | Jiang XX, Shen H, He TT. Centralized central air-conditoning cooling towers of water pollution condition of Legionella bacteria and analysis of strain type[J]. Chinese Journal of Health Laboratory Technology, 2009, 19(1): 185–186. (in Chinese) 蒋兴祥, 沈红, 何婷婷. 集中式中央空调冷却塔水军团菌污染状况及菌型分析[J]. 中国卫生检验杂志, 2009, 19(1): 185–186. |
| [11] | Zhou HJ, Ren HY, Zhu BQ, et al. Optimization of pulsed-field gel electrophoresis for Legionella pneumophila subtyping[J]. Appl Environ Microbiol, 2010, 76(5): 1334–1340. DOI:10.1128/AEM.01455-09 |
| [12] | Wang LL, Xu JG. Application of pulsed field gel electrophoresis (PFGE) in molecular typing[J]. Disease Surveillance, 2006, 21(5): 276–279. (in Chinese) 王丽丽, 徐建国. 脉冲场凝胶电泳技术(PFGE)在分子分型中的应用现状[J]. 疾病监测, 2006, 21(5): 276–279. |
| [13] | Mortensen ES, Fenton KA, Rekviq OP. Lupus nephritis:the central role of nucleosomes revealed[J]. Am J Pathol, 2008, 172(2): 275–283. DOI:10.2353/ajpath.2008.070563 |
| [14] | Chen M, Chen ML, Wang GY, et al. Genotyping Study on Some Strains of Legionella pneumophila Serotype 1 in Shanghai by Pulsed-field Gel Electrophoresis[J]. J Environ Occup Med, 2010, 27(6): 356–358. (in Chinese) 陈敏, 陈明亮, 王刚毅, 等. 2007年上海市部分嗜肺军团菌血清1型菌株PFGE分型研究[J]. 环境与职业医学, 2010, 27(6): 356–358. |
| [15] | Yuan YM, Yuan M, Yu MH. Analysis of fingerprinting of Legionella pneumophila serogroup 1 strains by pulsed field gel electrophoresis[J]. Journal of Tropical Medicine, 2008, 8(6): 889–890. (in Chinese) 袁月明, 袁梦, 俞慕华. 深圳市嗜肺军团菌血清1型菌株PFGE分型指纹图谱研究[J]. 中国热带医学, 2008, 8(6): 889–890. |
 2017, Vol. 32
2017, Vol. 32


