扩展功能
文章信息
- 王秀云, 王海红, 王涛, 张丽文, 杨俊英, 朱宗龙, 张梦洁
- WANG Xiu-yun, WANG Hai-hong, WANG Tao, ZHANG Li-wen, YANG Jun-ying, ZHU Zong-long, ZHANG Meng-jie
- 2008-2015年北京市昌平区疑似预防接种异常反应分析
- Analysis on adverse events following immunization in Changping district, Beijing 2008-2015
- 疾病监测, 2017, 32(6): 494-499
- Disease Surveillance, 2017, 32(6): 494-499
- 10.3784/j.issn.1003-9961.2017.06.013
-
文章历史
- 收稿日期:2017-03-28
疑似预防接种异常反应(adverse events following immunization,AEFI)是指在预防接种后发生的怀疑与预防接种有关的反应或事件[1]。随着免疫规划工作的发展,通过接种疫苗预防控制传染病得到广泛认可,近年疫苗种类不断增加,全国报告疫苗不良反应事件增多,使疫苗安全性及其AEFI发生情况引起广泛关注。北京市昌平区自2008年起开展AEFI监测网络报告工作,在《全国AEFI监测方案》(2010年)和《北京市疑似预防接种异常反应监测方案》(2014年)的指导下,昌平区AEFI监测系统各项指标报告情况逐年改善。为了解北京市昌平区AEFI发生情况及分布特征,现将2008—2015年该地AEFI监测数据进行分析,报告如下。
1 资料与方法1.1 资料来源2008—2015年北京市昌平区AEFI个案资料来源于“全国AEFI信息管理系统”,疫苗接种资料来源于“中国免疫规划监测信息管理系统”(national immunization program information management system,NIPIMS)。
1.2 AEFI监测范围分析数据为2008—2015年北京市昌平区报告的接种国家免疫规划(national immunization program,NIP)疫苗和非NIP疫苗的所有人群中发生的AEFI个案数据。
1.3 AEFI调查诊断和分类根据《全国AEFI监测方案》和《北京市疑似预防接种异常反应监测方案》对AEFI进行调查和因果关联评价。AEFI按发生原因分类为不良反应(包括一般反应和异常反应)、疫苗质量事故、接种事故、偶合症和心因性反应。
1.4 资料整理与分析应用Excel和SPSS软件对数据进行整理,采用描述性分析方法,对AEFI分布特征和相关指标进行流行病学分析。
1.5 分析指标某疫苗AEFI报告发生率(/10万剂)=该疫苗报告AEFI数/该疫苗接种剂次数×10万剂。
1.6 AEFI评价指标以省(区、市)为单位,AEFI在发现后48 h内报告率≥90%[1],以区(县)为单位,AEFI发现后24 h报告率≥90%[2];需要调查的AEFI在报告后48 h内调查率≥90%[1-2];AEFI个案调查表在调查后3 d内系统录入率≥100%[2];AEFI报告的接种单位报告覆盖率达到100%[2]。
2 结果2.1 AEFI报告及分类情况2008—2015年北京市昌平区实施预防接种8 013 332剂次,共报告AEFI病例926例,AEFI总报告发生率为11.56/10万剂次。其中一般反应472例,发生率5.98/10万剂次,占50.97%;异常反应326例,发生率4.07/10万剂次,占35.21%;偶合反应116例,发生率1.45/10万剂次,占12.53%;心因性反应4例,发生率0.05/10万剂次,占0.43%;不明原因1例,发生率0.01/10万剂次,占0.11%;无疫苗质量事故和接种事故。
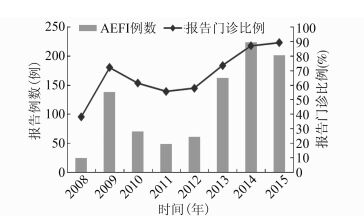
AEFI发生率总体呈现波动趋势,2008年AEFI报告数(24例)和发生率(2.94/10万剂次)最低,2014年报告数(224例)和发生率(20.59/10万剂次)最高,见图 1。分年度AEFI报告病例分类中,一般反应也呈现2008年报告数和发生率最低,2014年最高的现象。而异常反应则呈现2011年报告数最低,2014年报告数最高的现象,见表 1。
|
| 图 1 2008—2015年北京市昌平区疑似预防接种异常反应报告病例数和接种门诊报告比例 Figure 1 Reported AEFI case number and reporting rate of vaccination clinics in Changping, 2008-2015 |
| |
| 年份 | 一般反应 | 异常反应 | 偶合症 | 心因性反应 | 不明原因 | 总计 | ||||||
| 个案数 | 发生率 (/10万剂次) | 个案数 | 发生率 (/10万剂次) | 个案数 | 发生率 (/10万剂次) | 个案数 | 发生率 (/10万剂次) | 个案数 | 发生率 (/10万剂次) | 个案数 | 发生率 (/10万剂次) | |
| 2008 | 11 | 1.35 | 13 | 1.59 | 0 | 0.00 | 0 | 0.00 | 0 | 0.00 | 24 | 2.94 |
| 2009 | 63 | 7.71 | 35 | 3.22 | 38 | 3.50 | 1 | 0.09 | 0 | 0.00 | 137 | 12.60 |
| 2010 | 23 | 2.81 | 28 | 2.82 | 20 | 2.01 | 0 | 0.00 | 0 | 0.00 | 71 | 7.14 |
| 2011 | 25 | 3.06 | 12 | 1.34 | 11 | 1.23 | 0 | 0.00 | 0 | 0.00 | 48 | 5.36 |
| 2012 | 22 | 2.69 | 30 | 2.80 | 8 | 0.75 | 0 | 0.00 | 0 | 0.00 | 60 | 5.60 |
| 2013 | 99 | 12.11 | 46 | 4.48 | 14 | 1.36 | 2 | 0.19 | 0 | 0.00 | 161 | 15.68 |
| 2014 | 126 | 15.41 | 84 | 7.72 | 12 | 1.10 | 1 | 0.09 | 1 | 0.09 | 224 | 20.59 |
| 2015 | 110 | 13.46 | 78 | 7.55 | 13 | 1.26 | 0 | 0.00 | 0 | 0.00 | 201 | 19.46 |
| 合计 | 479 | 5.98 | 326 | 4.07 | 116 | 1.45 | 4 | 0.05 | 1 | 0.01 | 926 | 11.56 |
2008—2015年北京市昌平区46家预防接种门诊均有AEFI报告,分年度接种门诊报告率均未达到《北京市疑似预防接种异常反应监测方案》100%的要求,但报告水平逐步提高:2008年接种门诊报告率仅为38%,2009年升高至72%,20102012年有所降低;2013年开始接种门诊报告率逐渐升高,2015年为89%,达到最高水平(图 1)。
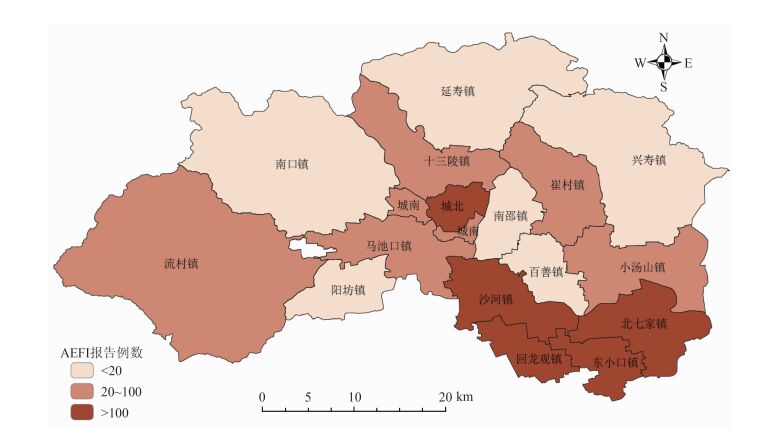
2.2 AEFI的流行病学特征2008—2015年北京市昌平区所辖的20个街镇均有AEFI报告,累计报告较多的主要为与海淀、朝阳接壤的北七家、回龙观、东小口、沙河等南部街镇及昌平城区(城北街道),其中报告最多的为回龙观镇,共173例,报告最少的为延寿镇,共7例,各街镇AEFI报告例数差距明显,见图 2。
|
| 图 2 2008—2015年北京市昌平区疑似预防接种异常反应报告病例街镇分布 Figure 2 Area distribution of AEFI cases in Changping, 2008-2015 |
| |
926例AEFI个案中,<1岁组349例(37.69%);1~6岁组435例(46.98%);>6岁组142例(15.33%);男女性别比为1.25:1。一般反应中,1~6岁组所占比例最高(59.50%),异常反应和偶合症中<1岁组所占比例最高。14季度均有AEFI病例报告,但第1季度AEFI发生比例明显低于其他3个季度,见表 2。
| 特征 | 一般反应 | 异常反应 | 偶合症 | 心因性反应 | 其他 | 总计 | ||||||
| 例数 | 构成比 % | 例数 | 构成比 % | 例数 | 构成比 % | 例数 | 构成比 % | 例数 | 构成比 % | 例数 | 构成比 % | |
| 性别 | ||||||||||||
| 男性 | 258 | 53.86 | 187 | 57.36 | 69 | 59.48 | 0 | 0.00 | 0 | 0.00 | 514 | 55.51 |
| 女性 | 221 | 46.14 | 139 | 42.64 | 47 | 40.52 | 4 | 100.00 | 1 | 100.00 | 412 | 44.49 |
| 年龄组(岁) | ||||||||||||
| <1 | 134 | 27.97 | 169 | 51.84 | 46 | 39.66 | 0 | 0.00 | 0 | 0.00 | 349 | 37.69 |
| 1~ | 285 | 59.50 | 119 | 36.50 | 30 | 25.86 | 0 | 0.00 | 1 | 100.00 | 435 | 46.98 |
| >6 | 60 | 12.53 | 38 | 11.66 | 40 | 34.48 | 4 | 100.00 | 0 | 0.00 | 142 | 15.33 |
| 季度 | ||||||||||||
| 1 | 70 | 14.61 | 56 | 17.18 | 15 | 12.93 | 1 | 25.00 | 0 | 0.00 | 142 | 15.33 |
| 2 | 141 | 29.44 | 93 | 28.53 | 23 | 19.83 | 0 | 0.00 | 0 | 0.00 | 257 | 27.75 |
| 3 | 137 | 28.60 | 109 | 33.44 | 31 | 26.72 | 1 | 25.00 | 0 | 0.00 | 278 | 30.02 |
| 4 | 131 | 27.35 | 68 | 20.86 | 47 | 40.52 | 2 | 50.00 | 1 | 100.00 | 249 | 26.89 |
| 合计 | 479 | 100.00 | 326 | 100.00 | 116 | 100.00 | 4 | 100.00 | 1 | 100.00 | 926 | 100.00 |
2008—2015年北京市昌平区报告的926例AEFI中,24 h内报告率为94.38%,48 h内报告率为96.76%,48 h内调查率为99.89%,调查后3 d内系统录入率为99.78%,见表 3。2010年《全国AEFI监测方案》实施后,2011年昌平区48 h内报告率和48 h内调查率均达到100%的工作要求。
| 年份 | 疑似预防接种 异常反应例数 | 接种门诊报告 比例(%) | 24 h内 报告率(%) | 48 h内 报告率(%) | 48 h内 调查率(%) | 调查后3 d内 系统录入率a |
| 2008 | 24 | 38.10 | 79.17 | 91.67 | 100.00 | - |
| 2009 | 138 | 72.09 | 80.43 | 88.41 | 99.28 | - |
| 2010 | 70 | 61.36 | 77.14 | 82.86 | 100.00 | - |
| 2011 | 48 | 55.56 | 95.83 | 100.00 | 100.00 | 100.00 |
| 2012 | 60 | 57.78 | 100.00 | 100.00 | 100.00 | 100.00 |
| 2013 | 162 | 73.33 | 100.00 | 100.00 | 100.00 | 100.00 |
| 2014 | 223 | 86.96 | 98.21 | 100.00 | 100.00 | 99.55 |
| 2015 | 201 | 89.13 | 100.00 | 100.00 | 100.00 | 100.00 |
| 合计 | 926 | 66.75 | 94.38 | 96.76 | 99.89 | 99.78 |
| 注:a 《全国AEFI监测方案》实施后,“AEFI信息管理系统”提出调查后3 d系统录入率≥100%的要求,故统计从2011年开始体现 | ||||||
2008—2015年北京市昌平区共实施接种27个疫苗,除抗狂犬病免疫球蛋白、无细胞百白破b型流感嗜血杆菌联合疫苗无AEFI报告外,其余25个疫苗均有AEFI报告,居前3位的疫苗依次为吸附无细胞百白破灭活脊髓灰质炎和b型流感嗜血杆菌(结合)联合疫苗(64.98/10万剂次)、麻疹风疹联合减毒活疫苗(54.19/10万剂次)和7价肺炎球菌多糖结合疫苗(36.35/10万剂次)。AEFI一般反应:平均发生率为5.89/10万剂次,其中接种吸附无细胞百白破灭活脊髓灰质炎和b型流感嗜血杆菌(结合)联合疫苗的发生率最高(45.87/10万剂次),流行性乙型脑炎灭活疫苗和霍乱疫苗发生率为零。AEFI异常反应:平均发生率为4.07/10万剂次,其中接种麻疹风疹联合减毒活疫苗发生率最高(39.56/10万剂次),卡介苗异常反应报告发生率最低(0.36/10万剂次),见表 4。
| 疫苗名称 | 接种 剂次 | 一般反应 | 异常反应 | 偶合症 (例数) | 心因性反应 (例数) | 其他 (例数) | 总计 | |||
| 例数 | 报告发生率 (/10万剂次) | 例数 | 报告发生率 (/10万剂次) | 例数 | 报告发生率 (/10万剂次) | |||||
| 吸附无细胞百白破灭活脊髓灰质炎和 b型流感嗜血杆菌(结合)联合疫苗 | 26 162 | 12 | 45.87 | 5 | 19.11 | 0 | 0 | 0 | 17 | 64.98 |
| 麻疹风疹联合减毒活疫苗 | 184 527 | 16 | 8.67 | 73 | 39.56 | 11 | 0 | 0 | 100 | 54.19 |
| 7价肺炎球菌多糖结合疫苗 | 49 525 | 12 | 24.23 | 4 | 8.08 | 2 | 0 | 0 | 18 | 36.35 |
| 无细胞百白破联合疫苗 | 784 021 | 201 | 25.64 | 31 | 3.95 | 16 | 0 | 0 | 248 | 31.63 |
| 麻疹减毒活疫苗 | 127 635 | 9 | 7.05 | 16 | 12.54 | 9 | 2 | 0 | 36 | 28.21 |
| 甲型流感疫苗 | 243 133 | 22 | 9.05 | 7 | 2.88 | 29 | 1 | 0 | 59 | 24.27 |
| 23价肺炎球菌多糖疫苗 | 79 088 | 8 | 10.12 | 8 | 10.12 | 1 | 0 | 0 | 17 | 21.50 |
| b型流感嗜血杆菌多糖结合疫苗 | 305 798 | 35 | 11.45 | 13 | 4.25 | 4 | 0 | 0 | 52 | 17.00 |
| 脊髓灰质炎(脊灰)灭活疫苗(Salk株) | 29 822 | 3 | 10.06 | 1 | 3.35 | 1 | 0 | 0 | 5 | 16.77 |
| 乙脑灭活疫苗 | 7 561 | 0 | 0.00 | 1 | 13.23 | 0 | 0 | 0 | 1 | 13.23 |
| A群脑膜炎球菌多糖疫苗 | 462 881 | 24 | 5.18 | 23 | 4.97 | 7 | 0 | 0 | 54 | 11.67 |
| 乙型脑炎(乙脑)减毒活疫苗 | 423 807 | 25 | 5.90 | 17 | 4.01 | 5 | 0 | 1 | 48 | 11.33 |
| 霍乱疫苗 | 10 098 | 0 | 0.00 | 1 | 9.90 | 0 | 0 | 0 | 1 | 9.90 |
| 狂犬病血清 | 51 616 | 0 | 0.00 | 5 | 9.69 | 0 | 0 | 0 | 5 | 9.69 |
| 水痘减毒活疫苗 | 238 331 | 10 | 4.20 | 12 | 5.04 | 1 | 0 | 0 | 23 | 9.65 |
| 白喉破伤风联合疫苗 | 239 838 | 18 | 7.51 | 1 | 0.42 | 3 | 0 | 0 | 22 | 9.17 |
| 口服轮状病毒减毒活疫苗 | 116 495 | 4 | 3.43 | 5 | 4.29 | 1 | 0 | 0 | 10 | 8.58 |
| 甲肝灭活疫苗 | 386 480 | 17 | 4.40 | 9 | 2.33 | 3 | 0 | 0 | 29 | 7.50 |
| 口服脊髓灰质炎(脊灰)减毒活疫苗 | 721 448 | 11 | 1.52 | 31 | 4.30 | 8 | 0 | 0 | 50 | 6.93 |
| 麻腮风联合减毒活疫苗 | 464 067 | 8 | 1.72 | 21 | 4.53 | 2 | 0 | 0 | 31 | 6.68 |
| A群C群脑膜炎球菌结合疫苗 | 318 473 | 9 | 2.83 | 9 | 2.83 | 0 | 0 | 0 | 18 | 5.65 |
| 流感疫苗 | 1 085 698 | 22 | 2.03 | 12 | 1.11 | 7 | 1 | 0 | 42 | 3.87 |
| 重组乙型肝炎疫苗 | 746 099 | 9 | 1.21 | 13 | 1.74 | 2 | 0 | 0 | 24 | 3.22 |
| 狂犬疫苗 | 604 324 | 3 | 0.50 | 7 | 1.16 | 3 | 0 | 0 | 13 | 2.15 |
| 卡介苗 | 274 916 | 1 | 0.36 | 1 | 0.36 | 1 | 0 | 0 | 3 | 1.09 |
| 抗狂犬病免疫球蛋白 | 31 458 | 0 | 0.00 | 0 | 0.00 | 0 | 0 | 0 | 0 | 0.00 |
| 无细胞百白破b型流感嗜血杆菌联合疫苗 | 30 | 0 | 0.00 | 0 | 0.00 | 0 | 0 | 0 | 0 | 0.00 |
| 合计 | 8 013 332 | 472 | 5.89 | 326 | 4.07 | 116 | 4 | 1 | 926 | 11.56 |
926例AEFI中,临床诊断以发热/红肿/硬结为主(449例,占48.49%),发生率为5.98/10万剂次;其次为过敏性皮疹(133例,占14.36%),发生率为1.66/10万剂次;荨麻疹(106例,占11.45%),发生率为1.32 /10万剂次,见表 5。
| 不良反应 | 例数 | 发生率 (/10万剂次) | 接种后天数(d) | ||||
| <1 | 1 | 2~5 | 6~15 | >15 | |||
| 一般反应 | 479 | 5.98 | 258 | 187 | 31 | 2 | 1 |
| 发热/红肿/硬结 | 449 | 5.60 | 244 | 177 | 27 | 0 | 1 |
| 其他 | 30 | 0.37 | 14 | 10 | 4 | 2 | 0 |
| 异常反应 | 326 | 4.07 | 209 | 64 | 31 | 16 | 6 |
| 斑丘疹 | 8 | 0.10 | 8 | 0 | 0 | 0 | 0 |
| 过敏反应-麻疹猩红热样皮疹 | 8 | 0.10 | 4 | 0 | 2 | 2 | 0 |
| 过敏性皮疹 | 133 | 1.66 | 89 | 26 | 14 | 4 | 0 |
| 过敏性休克 | 1 | 0.01 | 1 | 0 | 0 | 0 | 0 |
| 过敏性紫癜 | 4 | 0.05 | 1 | 1 | 1 | 1 | 0 |
| 卡介苗淋巴结炎 | 1 | 0.01 | 0 | 0 | 0 | 0 | 1 |
| 其他过敏反应 | 1 | 0.01 | 0 | 1 | 0 | 0 | 0 |
| 热性惊厥 | 6 | 0.07 | 6 | 0 | 0 | 0 | 0 |
| 无菌性脓肿 | 1 | 0.01 | 0 | 0 | 0 | 0 | 1 |
| 血管性水肿 | 16 | 0.20 | 6 | 7 | 3 | 0 | 0 |
| 血小板减少性紫癜 | 8 | 0.10 | 1 | 0 | 2 | 2 | 3 |
| 荨麻疹 | 106 | 1.32 | 79 | 22 | 5 | 0 | 0 |
| 其他 | 33 | 0.41 | 14 | 7 | 4 | 7 | 1 |
| 合计 | 805 | 10.05 | 467 | 251 | 62 | 18 | 7 |
926例AEFI中不良反应共805例,发生在接种后<1 d的467例(58.01%);接种后1 d的251例(31.18%);接种后2~5 d的62例(7.70%);接种后6~15 d的18例(2.34%);接种后>15 d的7例(0.87%),见表 5。
3 讨论2008—2015年北京市昌平区无疫苗质量事故和接种事故报告,AEFI报告呈上升趋势,接种门诊报告比例、及时报告率、及时调查率逐年提高,《全国AEFI监测方案》发布后,昌平区对基层工作人员进行强化培训,48 h报告率和调查率分别由2010年的82.86%和91.43%上升至2011年的100%。虽然昌平区AEFI街镇报告率达到100%,但接种门诊报告比例仅为89%,未达到《北京市疑似预防接种异常反应监测方案》100%的标准,少数接种量少的门诊可能全年无AEFI报告。提示昌平区需进一步细化考核评价指标、进行有针对性的培训以强化AEFI监测能力,提高AEFI报告覆盖率。
2008—2015年昌平区AEFI一般反应发生率为5.98/10万剂次,异常反应发生率为4.07/10万剂次,高于北京市2011年报告的5.85/10万剂次和2.32/10万剂次的平均水平,但与北京市其他区(县)的1.48/10万剂次~25.62/10万剂次(一般反应报告发生率)和0.58/10万剂次~11.22/10万剂次(异常反应报告发生率)相较仍处于较低水平[3]。昌平区报告的AEFI,一般反应所占比例(51.73%)明显低于全国2010—2013年平均水平(89.10%)[4-8],可能与部分症状较轻的一般反应患者未到接种单位就诊有关。
昌平区AEFI监测数据分析显示,最常见不良反应为发热、局部红肿和硬结,占总病例数的48.16%,其次是过敏性皮疹(14.36%),与全国报告情况类似。异常反应中过敏性皮疹所占比例较高(1.66/10万剂次),高于8.90/100万剂次~13.10/100万剂次的全国水平(2011—2013年)[4-6]。过敏性休克的发生率为0.01/10万剂次,低于0.04/100万剂次~0.20/100万剂次(2011—2013年)的全国水平[4-6],亦低于美国1991—2001年0.20/100万剂次的水平[9]。
2008—2015年昌平区AEFI一般反应和异常反应报告发生率较高的疫苗为吸附无细胞百白破灭活脊髓灰质炎和b型流感嗜血杆菌(结合)联合疫苗、7价肺炎球菌多糖结合疫苗、b型流感嗜血杆菌多糖结合疫苗等二类疫苗,与北京市顺义区及海淀区AEFI监测结果相似[10-11],考虑可能与疫苗特性及二类疫苗接种后AEFI的发生更受家长关注有关。麻疹风疹联合减毒活疫苗和麻疹减毒活疫苗是一类疫苗中一般反应和异常反应报告率较高的疫苗,考虑与近几年扩大免疫规划及加强成年人接种有关。无细胞百白破联合疫苗不良反应报告发生率为31.63/10万剂次,居昌平区25个疫苗AEFI发生率的第4位,同时也是报告AEFI例数最多的疫苗(248例,占926例病例的26.78%),可能与百日咳疫苗生物学性状[3-4]、接种剂次和接种人群等因素有关[6]。
作者贡献:
ORCID:0000-0003-4986-7054
王秀云:论文撰写,数据分析
王海红、王涛、张丽文、杨俊英、朱宗龙:数据收集
张梦洁:数据整理
| [1] |
Ministry of Health, State Food and Drug Administration of the People's Republic of China. National guideline for the surveillance of adverse events following immunization[S].Beijing:Ministry of Health, 2010. (in Chinese)
卫生部, 国家食品药品监督管理局. 全国疑似预防接种异常反应监测方案[S]. 北京: 卫生部, 2010. |
| [2] |
Pang XH, Lu L.
Technical specification for vaccination in Beijing[M]. Beijing: Science Press, 2014.
(in Chinese) 庞星火, 卢莉. 北京市预防接种工作技术规范[M]. 北京: 科学出版社, 2014. |
| [3] |
Sun MP, Gu KC, Miao L, et al.
Evaluation of operating quality of Adverse Events Following Immunization surveillance system and analysis of the reported cases in Beijing during 2011[J].
Adverse Drug Reactions Journal, 2012, 14(6): 345–351.
(in Chinese) 孙美平, 顾凯辰, 苗良, 等. 2011年北京市疑似预防接种异常反应监测系统运行质量评价与报告病例分析[J]. 药物不良反应杂志, 2012, 14(6): 345–351. |
| [4] |
Wu WD, Li KL, Zheng JS, et al.
Analysis on surveillance data of adverse events following immunization in China, 2011[J].
Chinese Journal of Vaccines and Immunization, 2013, 19(2): 97–109.
(in Chinese) 武文娣, 李克莉, 郑景山, 等. 中国2011年疑似预防接种异常反应监测数据分析[J]. 中国疫苗和免疫, 2013, 19(2): 97–109. |
| [5] |
Wu WD, Liu DW, Li KL, et al.
Analysis on surveillance data of adverse events following immunization in China, 2012[J].
Chinese Journal of Vaccines and Immunization, 2014, 20(1): 1–12, 66.
(in Chinese) 武文娣, 刘大卫, 李克莉, 等. 中国2012年疑似预防接种异常反应监测数据分析[J]. 中国疫苗和免疫, 2014, 20(1): 1–12, 66. |
| [6] |
Ye JK, Li KL, Xu DS, et al.
Evaluation of the adverse events following immunization information management system in China, 2013[J].
Chinese Journal of Vaccines and Immunization, 2015, 21(2): 121–131, 200.
(in Chinese) 叶家楷, 李克莉, 许涤沙, 等. 中国2013年疑似预防接种异常反应信息管理系统数据分析[J]. 中国疫苗和免疫, 2015, 21(2): 121–131, 200. |
| [7] |
Ye JK, Li KL, Xu DS, et al.
Analysis of surveillance for adverse events following immunization in China, 2014[J].
Chinese Journal of Vaccines and Immunization, 2016, 22(2): 125–137.
(in Chinese) 叶家楷, 李克莉, 许涤沙, 等. 中国2014年疑似预防接种异常反应信息管理系统监测数据分析[J]. 中国疫苗和免疫, 2016, 22(2): 125–137. |
| [8] |
Wu WD, Liu DW, Li KL, et al.
Analysis on adverse events following immunization surveillance in China, 2010[J].
Chinese Journal of Vaccines and Immunization, 2012, 18(5): 385–397.
(in Chinese) 武文娣, 刘大卫, 李克莉, 等. 中国2010年疑似预防接种异常反应监测数据分析[J]. 中国疫苗和免疫, 2012, 18(5): 385–397. |
| [9] | Zhou WG, Pool V, Iskander JK, et al. Surveillance for safety after immunization:Vaccine Adverse Event Reporting System (VAERS)-United States, 1991-2001[J]. MMWR Surveill Summ, 2003, 52(1): 1–24. |
| [10] |
Xiao L, Wang FS, Tang Y, et al.
Surveillance and analysis of adverse events following immunization in 2008-2014 in Shunyi district, Beijing[J].
Chinese Journal of Biologicals, 2016, 29(4): 403–406, 412.
(in Chinese) 肖雷, 王凤双, 唐莹, 等. 北京市顺义区2008-2014年疑似预防接种异常反应监测分析[J]. 中国生物制品学杂志, 2016, 29(4): 403–406, 412. |
| [11] |
Xu RH, Cai R, Fu JY, et al.
Surveillance and analysis on the suspected adverse events following immunization in Haidian district, Beijing in 2012[J].
Practical Preventive Medicine, 2014, 21(7): 814–817.
(in Chinese) 徐若辉, 蔡润, 富继业, 等. 北京市海淀区2012年疑似预防接种异常反应监测分析[J]. 实用预防医学, 2014, 21(7): 814–817. |
 2017, Vol. 32
2017, Vol. 32


