扩展功能
文章信息
- 连健
- LIAN Jian
- 福建省长乐市80株结核分枝杆菌临床分离株可变数目串联重复序列基因分型研究
- Multiple-locus variable number tandem repeat analysis on genotypes of 80 strains of Mycobacterium tuberculosis in Changle, Fujian province
- 疾病监测, 2014, 29(10): 797-801
- Disease Surveillance, 2014, 29(10): 797-801
- 10.3784/j.issn.1003-9961.2014.10.011
-
文章历史
- 收稿日期:2014-06-03
传统的流行病学方法不能很好地揭示结核病的传播规律,分子生物学与流行病学研究方法相结合产生的分子流行病学在这方面有着不可替代的优势。多位点数目可变串联重复序列分析(MLVA,multiple loci VNTR analysis)是利用基因组中特定位点上可变数目串联重复序列(variable number of tandem repeats,VNTRs)进行基因型分型[1]。
本研究选取15个VNTR位点,对福建省长乐市医院2013年结核病患者痰标本中分离的80株结核分枝杆菌进行基因分型研究,初步探讨长乐市结核分枝杆菌VNTR的分布特征、基因分型和流行株,为结核病防治工作提供分子流行病学依据。 1材料与方法 1.1材料 1.1.1样本来源收集
从2013年1月至2013年12月,长乐市医院检验科微生物实验室试验的涂阳肺结核患者痰标本临床分离株共80株,经对硝基苯甲酸(PNB)、噻吩-2-羧酸肼(TCH)鉴别培养基初步鉴别为结核分枝杆菌。结核分枝杆菌标准株H37Rv由国家结核病参比室提供,作为本次试验的对照菌株。80株菌株对应患者资料取自中国结核病信息管理系统2013年长乐市网报资料、长乐市医院2013年登记报告常住人口和流动人口结核病患者的个案数据库资料,包括患者的基本信息、诊断和治疗管理信息。共登记患者80例,其中常住人口患者41例,流动人口患者39例。 1.1.2主要试剂
4种抗结核药物异烟肼(INH,H)、链霉素(SM,S)、利福平(RFP,R)、乙胺丁醇(EMB,E)购自成都锦华药业有限责任公司,2×PCR-Mix(2倍PCR预混液)购自Genestar公司,100 bp DNA ladder购自Genestar公司,Taq DNA聚合酶、dNTP购自华美生物工程公司。 1.2方法 1.2.1培养基制备
①基础培养基:无淀粉改良罗氏培养基,配方及制备方法按照《结核病诊断实验室检验规程》[2](以下简称《规程》)进行。②含药培养基:RFP、EMB、SM和INH溶解、稀释浓度均参照《规程》。含药培养基无菌分装7 ml/管,斜置于培养基蒸汽凝固灭菌箱内,85 ℃凝固50 min。制成的培养基37 ℃无菌试验24 h,检查无污染后,4 ℃避光保存,1个月内使用。定义:耐多药(multi-drug resistance,MDR): 指结核分枝杆菌至少对异烟肼、利福平2种及以上抗结核药物耐药[3]。 1.2.2药物敏感性试验
80株结核分枝杆菌用采用WHO/IUATLD《结核病耐药检测指南》[4]推荐的比例法测试其对药物敏感性。①菌悬液制备:刮取菌龄2~3周的结核分枝杆菌菌落(刮取斜面各个部分培养物),放玻璃磨菌器内研磨,以0.5%吐温-80生理盐水稀释,与标准麦氏比浊管比浊,配成1 mg/ml菌悬液。②比例法:试验方法同《规程》。制备1 mg/ml菌悬液,用22SWG标准接种环将菌液逐步稀释至10-2和10-4 mg/ml(22SWG标准接种环:金属丝直径0.7 mm,金属丝内径3 mm,一满环可移菌液0.01 ml)。用22SWG标准接种环分别沾取一满环(即0.01 ml)10-2和10-4mg/ml的菌液。用划线法均匀接种至对照及含药培养基斜面。最终接菌量为10-4和10-6 mg。37 ℃培养4周后观察结果并计算耐药百分比:耐药百分比=(含药培养基上生长的菌落数)∕(对照培养基上生长的菌落数)×100%。若耐药百分比>1%,则认为受试菌对该药耐药(R),<1%判断为敏感(S)。 1.2.3质量控制
每批试验用结核分枝杆菌参考菌株(H37Rv敏感株)10-3 mg检测含药培养基质量。本实验室(福建省疾病预防控制中心结核病防治所)每年均接受一次跨国参比实验室的分枝杆菌药敏试验室间质控,按照《世界卫生组织(WHO)/国际防痨和肺病联合会(IUATLD)结核病耐药监测指南》提出的INH及RFP一致率不应低于90%的要求,均达到标准。 1.2.4结核分枝杆菌DNA的制备
将结核分枝杆菌临床分离株常规接种于改良罗氏培养基,37 ℃ 培养2~4周,至有菌落生长后,取一环菌于400 μl TE中悬菌,100 ℃煮沸15 min,12 000 r/min离心10 min后,上清液用于基因分型实验。 1.2.5MLVA检测引物设计与合成
据参考文献报道[5, 6]和结核分枝杆菌基因数据库,初步筛选15个串联重复基因位点,见表 1。引物[7]由上海生工基因技术有限公司合成。
| 编号 | 位点名称 | 引物序列 |
| 1 | ETR-A | L)5′-ATT TCG ATC GGG ATG TTG AT-3′ |
| R)5′-TCG GTC CCA TCA CCT TCT TA-3′ | ||
| 2 | ETR-B | L)5′-GCG AAC ACC AGG ACA GCA TCA TG-3′ |
| R)5′-GGC ATG CCG GTG ATC GAG TGG-3′ | ||
| 3 | ETR-C | L)5′-GAC TTC AAT GCG TTG TTG GA-3′ |
| R)5′-GTC TTG ACC TCC ACG AGT GC-3′ | ||
| 4 | ETR-D | L)5′-GCG CGA GAG CCC GAA CTG C-3′ |
| R)5′-GCG CAG CAG AAA CGT CAG C-3′ | ||
| 5 | ETR-E | L)5′-ACT GAT TGG CTT CAT ACG GCT TTA-3′ |
| R)5′-GTG CCG ACG TGG TCT TGA T-3′ | ||
| 6 | MIRU10 | L)5′-GTT CTT GAC CAA CTG CAG TCG TCC-3′ |
| R)5′-GCC ACC TTG GTG ATC AGC TAC CT-3′ | ||
| 7 | MIRU16 | L)5′-TCG GTG ATC GGG TCC AGT CCA AGT A-3′ |
| R)5′-CCC GTC GTG CAG CCC TGG TAC-3′ | ||
| 8 | MIRU23 | L)5′-CAG CGA AAC GAA CTG TGC TAT CAC-3′ |
| R)5′-CGT GTC CGA GCA GAA AAG GGT AT-3′ | ||
| 9 | MIRU26 | L)5′-CCC GCC TTC GAA ACG TCG CT-3′ |
| R)5′-TGG ACA TAG GCG ACC AGG CGA ATA-3′ | ||
| 10 | MIRU27 | L)5′-TCG AAA GCC TCT GCG TGC CAG TAA-3′ |
| R)5′-GCG ATG TGA GCG TGC ACT CAA-3′ | ||
| 11 | MIRU39 | L)5′-CGC ATC GAC AAA CTG GAG CCA AAC-3′ |
| R)5′-CGG AAA CGT CTA CGC CCC ACA CAT-3′ | ||
| 12 | MIRU40 | L)5′-AAG CGC AAG AGC ACC AAG-3′ |
| R)5′-GTG GGC TTG TAC TTG CGA AT-3′ | ||
| 13 | Mtub21 | L)5′-AGA TCC CAG TTG TCG TCG TC-3′ |
| R)5′-CAA CAT CGC CTG GTT CTG TA-3′ | ||
| 14 | Mtub30 | L)5′-AGT CAC CTT TCC TAC CAC TCG TAA C-3′ |
| R)5′-ATT AGT AGG GCA CTA GCA CCT CAA G-3′ | ||
| 15 | Mtub39 | L)5′-AAT CAC GGT AAC TTC CCT TGT TT-3′ |
| R)5′-GAT GCA TGT TCG ACC CGT AG-3′ |
运用实时荧光定量-聚合酶链反应(real-time fluorescence quantitative-polymerase chain reaction,real-time FQ-PCR)方法。采用25 μl PCR反应体系,其中包括2 ng模板DNA、1.5 mmol/L MgCl2,0.2 mmol dNTP、上下游引物共30 pmol和1.5 U Taq DNA酶。分别用15对引物进行PCR扩增。PCR反应条件:预变性94 ℃ 10 min;循环94 ℃ 1 min,62 ℃ 1 min,72 ℃ 1.5 min,共40个循环;最后延伸72 ℃ 10 min;4 ℃保存。 1.2.7琼脂糖凝胶电泳
取3 μl PCR产物,在2%的琼脂糖凝胶上电泳,电泳电压采用10 V/cm,电泳40 min,将凝胶放入浓度为0.5 μg/ml的EB染色液中,染色30 min,自来水脱色5 min。之后,在紫外凝胶成像分析系统下观察结果,用100 bp DNA Marker来确定相对分子质量的大小,以标准菌株H37Rv作为对照[8, 9]。用Gel-Pro analyzer 4.0软件分析各PCR产物的分子质量大小并计算出各菌株的重复次数。 1.2.8统计学方法
采用SPSS 17.0软件进行统计分析,采用χ2检验比较相关性。用BioNumerics 5.0 软件对菌株进行聚类分析。 2结 果 2.1一般情况
80株结核分枝杆菌来源于福建省长乐市医院检验科微生物实验室试验的涂阳肺结核患者痰标本临床分离株,其中分离自流动人口39株、常住人口41株,登记患者的来源均以转诊为主,均占50%以上,健康体检所占的比例较低,见表 2。初治69株,复治11株,39例流动人口结核病例情况均为初治,常住人口也以初治为主,见表 3。80例结核病病例的性别和年龄结果显示,患者年龄16~81岁,男性(47例)多于女性(33例),以青壮年为主。在39例流动人口的职业分布中,农民工15例,占38.46%;其次为家政服务6例,工人4例,分别占15.38%和10.26%。
| 人口 类别 | 因症就诊 | 转诊 | 接触者检查 | 健康体检 | 合计 例数 | ||||
| 例数 | 构成比(%) | 例数 | 构成比(%) | 例数 | 构成比(%) | 例数 | 构成比(%) | ||
| 常住 | 18 | 43.90 | 21 | 51.22 | 0 | 0.00 | 2 | 4.88 | 41 |
| 流动 | 15 | 38.46 | 24 | 61.54 | 0 | 0.00 | 0 | 0.00 | 39 |
| 人口 类别 | 初治 | 复治 | 总计 | ||
| 例数 | 构成比(%) | 例数 | 构成比(%) | ||
| 常住 | 30 | 73.17 | 11 | 26.83 | 41 |
| 流动 | 39 | 100.00 | 0 | 0.00 | 39 |
| 合计 | 69 | 11 | 80 | ||
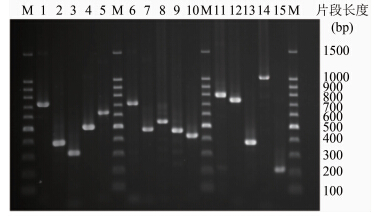
本研究共选取了l5个VNTR基因位点对80株结核分枝杆菌菌株进行基因分型,结果显示不同菌株的DNA指纹图谱呈现出明显多态性,见图 1、2。
|
| 注:M:分子质量标准; 1~15分别为Mtub 04、ETRC、MIRU 04(ETRD)、MIRU 40、MIRU 10、MIRU 16、Mtub 21、QUB-11b、ETRA、Mtub 30、MIRU 26、MIRU 31(ETRE)、Mtub 39、QUB-26、QUB-4156。 图 1 株结核分枝杆菌菌株的15个不同VNTR位点的 多态性检测结果 Figuer 1 Polymorphisms of 1 M. tuberculosis strain by 15 loci-VNTR genotyping |
|
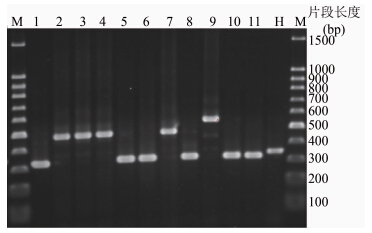
| 注:M:500 bp DNA ladder;H:H37Rv;1~11: 临床分离株。 图 2 部分结核分枝杆菌菌株在Mtub21 位点多态性检测结果 Figuer 2 Polymorphisms of some M. tuberculosis strains by 21 loci-VNTR genotyping |
80株结核分枝杆菌经软件聚类分析后被分为Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅶ、Ⅷ 7大基因群,分别包含菌株59、12、1、3、1、2和2株菌,其中最大的基因簇Ⅰ型共包含59(73.8%)株结核分枝杆菌;在株水平分类上80株结核分枝杆菌被分为77个基因型,其中74株为单菌株独立基因型,其余6株菌成2簇,各包含3株菌。 2.4不同特征人口结核分枝杆菌菌株分布
流动人口与常住人口的结核分枝杆菌VNTR基因型存在一定差异,见表 4,但均以Ⅰ型为主。流动人口结核分枝杆菌基因簇为Ⅰ、Ⅱ、Ⅳ、Ⅶ、Ⅷ,常住人口为Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅷ。
| 基因群 | 总株数 | 流动人口 | 常住人口 |
| Ⅰ | 59 | 28 | 31 |
| Ⅱ | 12 | 7 | 5 |
| Ⅲ | 1 | 0 | 1 |
| Ⅳ | 3 | 1 | 2 |
| Ⅴ | 1 | 0 | 1 |
| Ⅶ | 2 | 2 | 0 |
| Ⅷ | 2 | 1 | 1 |
在本次分析的80株结核分枝杆菌中,61%(49/80)表现全敏感,而39%(31/80)表现为耐药;在Ⅰ群菌株中,69.5%表现为全敏感,而30.5%(18/59)表现为耐药,经χ2检验,见表 5,菌型的分布与药敏间的差异无统计学意义(χ2=4.872,P>0.05)。
| 基因群 | 敏感菌株数 | 耐药菌株数 | 总计 |
| Ⅰ | 41 | 18 | 59 |
| Ⅱ | 1 | 11 | 12 |
| Ⅲ | 1 | 0 | 1 |
| Ⅳ | 2 | 1 | 3 |
| Ⅴ | 1 | 0 | 1 |
| Ⅶ | 1 | 1 | 2 |
| Ⅷ | 2 | 0 | 2 |
| 合计 | 49 | 31 | 80 |
在Ⅰ群菌株中,耐药30.5%(18/59),其中耐INH 15.25%(9/59),耐RFP 11.86%(7/59),耐SM 25.4%(15/59),耐EMB 5.1%(3/59),耐多药(MDR[8])5.1%(3/59),但其耐药性与其他基因群的差异无统计学意义,且Ⅰ群菌株与其他基因群相比在性别方面差异也无统计学意义。 3讨论
MLVA 基因分型是目前应用较多且成熟的方法[9, 10],其基本原理是对结核分枝杆菌基因组中存在的VNTR进行检测,通过计算各个VNTR位点的重复片段数目而将其分型。本研究采用该方法,初步探讨长乐市结核分枝杆菌MLVA 基因分型的分布特征,为长乐市肺结核病控制提供科学的分子流行病学等参考依据。
80株结核分枝杆菌MLVA分型结果显示,可分为Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅶ、Ⅷ 7大基因群,分别包含菌株59、12、1、3、1、2和2株菌,其中最大的基因簇Ⅰ型共包含59(73.8%)株结核分枝杆菌,所有的基因型与标准菌株H37Rv均不同型;在株水平分类上80株结核分枝杆菌被分为77个基因型,其中74株为单菌株独立基因型,其余6株菌成2簇,各包含3株菌。
本研究的80株结核分枝杆菌菌株,其中分离自流动人口39株(48.8%)。分析结果表明所有菌株可分成7个主要基因群,大部分菌株属于Ⅰ群(59株,73.8%),说明这些菌株属于一个亲缘关系很近的克隆系,可能为主要流行菌株,应加强对这类菌株的研究和监测。比较流动人口与常住人口结核分枝杆菌菌株的MLVA基因分型分布情况,发现均以Ⅰ型为主,说明流动人口与常住人口结核分枝杆菌流行特征相似。但同时也发现流动人口还存在部分不同于常住人口的基因型Ⅶ型,这可能与流动人口中以四川、重庆、江西等省份居多有关[11],应引起重视,必须加强监测。39例流动人口结核病患者的感染情况均为初治,职业以农民工居多,有15例(15/39),其次为家政服务人员,有6例(6/39)。此结果与杜昕等[12]的研究结果相同,由于外来流动人口以青壮年为主,活动能力大,经济收入普遍不高,居住处所不稳定,且健康和卫生意识较差,作为传染源,传播隐患更强。青壮年人群在促进长乐市经济发展的同时,也成为传染病发病的高危人群。加强长乐市流动人口结核病防治工作的紧迫性已日益突出。
从耐药性的结果分析,在Ⅰ群菌株中,耐药30.5%(18/59),其中耐INH 15.25%(9/59),耐RFP 11.86%(7/59),耐SM 25.4%(15/59),耐EMB 5.1%(3/59),耐多药(MDR)5.1%(3/59),但其耐药性与其他基因群的差异无统计学意义,且Ⅰ群菌株与其他基因群相比在性别方面差异也无统计学意义。并且耐多药率(5.1%)低于福建省部分地市曾经的报告[13]。本次结核分枝杆菌的研究样本量偏少,尤其是结核病复治病例数偏少且未对各年龄层次进行结核分枝杆菌的耐药性进行监测,有待进一步研究。
( 志谢: 感谢福建省CDC和福建省长乐市CDC对本项监测工作的大力支持与协助。)
| [1] | Charles J, Gao Q. MIRU-new Mycobacterium tuberculosis genotyping method introduction [J].Chinese Journal of Antituberculosis,2005,27(3):189-191.(in Chinese) 查佳,高谦.MIRU-新的结核分枝杆菌基因型分型方法简介[J].中国防痨杂志,2005,27(3):189-191. |
| [2] | Chinese Antituberculosis Association Professional Committee. The diagnosis of tuberculosis based inspection procedures for laboratory [S]. Beijing: Chinese Education Press,2006.(in Chinese) 中国防痨协会基础专业委员会.结核病诊断实验室检验规程[S].北京:中国教育文化出版社,2006. |
| [3] | Journal of the National Symposium on drug-resistant tuberculosis [J]. Chinese Journal of Tuberculosis and Respiratory,2002,23(2):79.(in Chinese) 全国耐药结核病学术研讨会纪要[J].中华结核和呼吸杂志,2002,23(2):79. |
| [4] | World Health Organization/International Union Against Tuberculosis and Lung Diseases, Guidelines for surveillance of drug resistance in tuberculosis [R].Geneva:WHO, 1997. |
| [5] | Parwati I, Vancrevel R, Van Sollingen D. Possible underlying mechanisms for successful emergence of the Mycobacterium tuberculosis Beijing genotype strains[J].Lancet,2010,2:456-457. |
| [6] | Lai CC,Tan CK,Lin SH, et al. Molecular evidence of false-positive cultures for Mycobacterium tuberculosis in a Taiwanese hospital with a high incidence of TB[J].CHEST,2010,137(5):1065-1070. |
| [7] | Zhu HY, Wu F, Qian XQ, et al. Haining clinical isolates of Mycobacterium tuberculosis MLVA genotyping study 2008 [J]. Chinese Rural Health Service Administration,2010,30(11):939-941.(in Chinese) 朱海燕,吴方,钱雪琪,等.海宁市2008年结核分枝杆菌临床分离株MLVA基因分型研究[J].中国农村卫生事业管理,2010,30(11):939-941. |
| [8] | Liang QF, Chen QY, Zhao Y, et al. The initial smear positive pulmonary tuberculosis drug resistance monitoring analysis of [J]. China Tropical Medicine,2011,11(12):1460-1466.(in Chinese) 梁庆福,陈求扬,赵永,等.初治涂阳肺结核患者耐药监测分析[J].中国热带医学,2011,11(12):1460-1466. |
| [9] | Yang Y, Dong HY, Li DY, et al. Genotyping of Mycobacterium Tuberculosis isolates in Sichuan province with spoligotpying[J]. Mycobacterium Tuberculosis,2012,41(5):28-31.(in Chinese) 杨筠,董海燕,李定越,等.四川省106株结核分枝杆菌spoligotyping基因分型研究[J].医学研究杂志,2012,41(5): 28-31. |
| [10] | Wang J, Huang YF, Zhang AH, et al. 101 children with tuberculosis clinical isolates of Mycobacterium tuberculosis multilocus variable number tandem repeat typing [J]. Journal of Third Military Medical University,2011,33(13):1408-1410.(in Chinese) 王均,黄延风,张爱华,等.儿童结核病101例临床分离结核分枝杆菌多位点串联重复序列分型[J].第三军医大学学报,2011,33(13):1408-1410. |
| [11] | Li X, Zhu Y. Analysis of the status of floating population in Fujian province[J].Journal of Fujian Normal University:Philosophy and Social Sciences Edtion,2004(5):45-51.(in Chinese) 李晓,朱宇.福建省流动人口状况分析[J].福建师范大学学报:哲学社会科学版,2004(5):45-51. |
| [12] | Du X, Liu EY, Chen W, et al. 2010 national resident population mobility and smear-positive tuberculosis patients transferred the management and treatment outcomes of comparative analysis [J].Chinese Journal of Antituberculosis,2011,33(9):527-530.(in Chinese) 杜昕,刘二勇,陈伟,等. 2010年全国流动和常住人口涂阳肺结核患者转出与治疗管理结局的对比分析[J].中国防痨杂志,2011,33(9):527-530. |
| [13] | Zheng RR, Zhang XD, Huang CJ. 875 strains of Mycobacterium tuberculosis drug resistance situation analysis [J]. Modern Preventive Medicine,2008,35(23):4697-4698.(in Chinese) 郑蓉蓉,张向东,黄成基.875株结核分枝杆菌耐药情况分析[J].现代预防医学,2008,35(23):4697-4698. |
 2014, Vol. 29
2014, Vol. 29


