扩展功能
文章信息
- 李马超, 刘海灿, 赵秀琴, 万康林
- LI Ma-chao, LIU Hai-can, ZHAO Xiu-qin, WAN Kang-lin
- 卡介苗中PE和PPE家族蛋白B细胞抗原表位多态性研究
- Polymorphism of B cell epitopes coded with PE/PPE gene family in BCG
- 疾病监测, 2016, 31(4): 282-287
- Disease Surveillance, 2016, 31(4): 282-287
- 10.3784/j.issn.1003-9961.2016.04.006
-
文章历史
- 收稿日期: 2015-12-10
结核病(Tuberculosis,TB)是由结核分枝杆菌(Mycobacterium tuberculosis,MTB)导致的慢性传染病。据世界卫生组织(WHO)统计,全球约有1/3的人感染结核,每年全球至少有170万人因TB而死亡[1]。中国是全球22个TB高负担国家之一,TB报告发病人数始终位居法定报告甲、乙类传染病前列[2]。
卡介苗(Bacille Calmette-Guérin,BCG)是由牛结核分枝杆菌连续传代培养而得到减毒活疫苗[3]。尽管BCG在人群中接种产生的保护效果存在较大争议,但BCG仍是迄今为止唯一在全球广泛使用的预防结核的疫苗[4]。尽管BCG对于预防和控制新生儿粟粒性结核和结核性脑膜炎等重症TB发挥了重要作用,但BCG刺激机体产生免疫保护的机制仍然不是十分清楚;且BCG在全球范围内的广泛使用,产生了多个不同的克隆,所具有的保护性抗原、理化性质、免疫特征等不同,所产生的免疫保护效果也存在差异[5]。
传统的观点认为TB的免疫以细胞免疫为主,但近期的研究表明B细胞主导的体液免疫反应对于刺激机体产生保护性抗体、调节宿主免疫应答方面起到重要作用[6, 7, 8]。B细胞抗原表位是抗原表面能够与B细胞识别并刺激B细胞产生抗体或分泌细胞因子调节免疫应答。PE和PPE基因家族为结核分枝杆菌基因组上特有的2个广泛存在的多基因家族[9]。研究表明PE和PPE家族蛋白的很多成员为细胞表面蛋白,与结核分枝杆菌的致病性相关,可以诱导机体产生体液免疫反应,甚至是作为新型结核疫苗的组成成分[10, 11, 12]。本研究通过对不同BCG基因组PE和PPE基因家族中B细胞抗原表位编码基因进行比较,试图从B细胞抗原表位的角度分析其在PE和PPE基因家族中分布差异以及可能对BCG保护力所产生的潜在影响。
1 材料与方法 1.1 菌株基因组数据来源对15株菌的全基因组数据进行比较分析。包括13株全球不同地区使用的BCG基因组数据,其中6株BCG菌株(BCG-Moreau、BCG-Phipps、BCG-Sweden、BCG-Prague、BCG-Glaxo、BCG-Frappier)购自中国药品生物制品检定所,全基因组测序工作由本实验室完成(采用illumina hiseq2000 V4测序平台,测序模式为100PE,测序数据量不低于基因组大小的900×);其余7株BCG基因组数据、1株结核分枝杆菌参考菌株(Mycobacterium tuberculosis H37Rv)和1株牛结核分枝杆菌参考菌株(Mycobacterium bovis AF2122/97)的基因组数据下载自美国国家生物技术信息中心(National Center for Biotechnology Information,NCBI)[13, 14, 15, 16, 17, 18, 19],见表 1。1.2结核分枝杆菌B细胞抗原表位在国际免疫表位数据库中(Immune Epitope Database,IEDB,http://www.iedb.org)检索结核分枝杆菌对于人的B细胞抗原表位序列,选择其中多肽表位序列作为本次研究对象。
| 菌株 | 大小(Mb) | GC% | 序列号 |
| BCG-Moreau | 4.16 | 0.654 | AKYS00000000 |
| BCG-Phipps | 4.14 | 0.654 | AKYT00000000 |
| BCG-Sweden | 4.09 | 0.653 | AKYV00000000 |
| BCG-Prague | 4.13 | 0.653 | AKYU00000000 |
| BCG-Glaxo | 4.21 | 0.654 | AKYR00000000 |
| BCG-Frappier | 4.24 | 0.655 | AKYQ00000000 |
| BCG-China | 4.18 | 0.653 | AEZE00000000 |
| BCG-Danish | 4.17 | 0.653 | AEZF00000000 |
| BCG-Russia | 4.18 | 0.653 | AEZG00000000 |
| BCG-Tice | 4.17 | 0.653 | AEZH00000000 |
| BCG-Mexico | 4.35 | 0.657 | NC_016804 |
| BCG-Pasteur | 4.37 | 0.656 | NC_008769 |
| BCG-Tokyo 172 | 4.37 | 0.656 | NC_012207 |
| M.tb H37Rv | 4.41 | 0.656 | NC_000962 |
| M.bovis AF2122/97 | 4.35 | 0.656 | NC_002945 |
将IEDB中收集到的结核分枝杆菌B细胞抗原表位多肽序列与结核分枝杆菌参考菌株(M.tb H37Rv)蛋白质组进行BLAST序列比对,以确定多肽表位的编码基因[20]。如果多肽表位序列与蛋白质组上多个位置完全匹配,将检索提交该表位的原始文献以确认编码基因。将编码B细胞抗原表位的基因根据其功能进行分类、确定PE/PPE基因家族[9]。
1.4 PE和PPE基因家族编码B细胞抗原表位在BCG以及牛结核分枝杆菌中的分布根据序列比对以及基因功能分类的结果,提取PE和PPE基因家族中编码B细胞抗原表位的核酸序列,并比较其在不同BCG菌株和M.bovis AF2122/97基因组中的分布。如果编码表位的核酸序列存在缺失,我们将设计引物对其完整的编码基因进行扩增测序验证。
2 结果 2.1 结核分枝杆菌特异性B细胞抗原表位通过检索IEDB,查询到经试验验证的结核分枝杆菌对于人的B细胞抗原多肽表位399个。由于其中2个表位(编号94762、94763)氨基酸组成序列相同、但存在不同的残基修饰,因此在本研究中选择其中1个(编号94762)作为代表。最终选择398个B细胞抗原表位作为研究对象。
2.2 B细胞抗原表位编码基因与功能分类通过序列比对,398个B细胞抗原表位分别由81个基因编码,根据功能分为9类;6个PE/PPE基因家族编码28个表位,占全部B细胞抗原表位的7.04%,见图 1。

|
| 图1 B细胞抗原表位在不同功能基因中的分布 Figure 1 Distribution of B cell epitopes in functional genes |
以6个PE/PPE基因家族序列为参考,与M.bovis AF2122/97基因组进行比对,确定等位基因在M.bovis中的基因分布,见表 2。
| 编号 | M.tb H37Rv | M.bovis AF2122/97 | 产物 |
| 121059 | Rv0755c | Mb0777c | PPE12 |
| 103198 | Rv0916c | Mb0940c | PE7 |
| 103420 | Rv0916c | Mb0940c | PE7 |
| 103007 | Rv1196 | Mb1228 | PPE18 |
| 103452 | Rv1196 | Mb1228 | PPE18 |
| 103365 | Rv1196 | Mb1228 | PPE18 |
| 103503 | Rv1196 | Mb1228 | PPE18 |
| 103737 | Rv2430c | Mb2456c | PPE41 |
| 9474 | Rv2608 | Mb2640 | PPE42 |
| 9475 | Rv2608 | Mb2640 | PPE42 |
| 10022 | Rv2608 | Mb2640 | PPE42 |
| 20281 | Rv2608 | Mb2640 | PPE42 |
| 21497 | Rv2608 | Mb2640 | PPE42 |
| 39354 | Rv2608 | Mb2640 | PPE42 |
| 44231 | Rv2608 | Mb2640 | PPE42 |
| 53833 | Rv2608 | Mb2640 | PPE42 |
| 55157 | Rv2608 | Mb2640 | PPE42 |
| 55158 | Rv2608 | Mb2640 | PPE42 |
| 103393 | Rv2608 | Mb2640 | PPE42 |
| 103022 | Rv3347c | Mb3380c | PPE55 |
| 103352 | Rv3347c | Mb3380c | PPE55 |
| 103038 | Rv3347c | Mb3379c | PPE55 |
| 19562 | Rv3347c | Mb3379c | PPE55 |
| 103469 | Rv3347c | Mb3380c | PPE55 |
| 103482 | Rv3347c | Mb3380c | PPE55 |
| 103645 | Rv3347c | Mb3379c | PPE55 |
| 103664 | Rv3347c | Mb3380c | PPE55 |
| 22387 | Rv3347c | Mb3380c | PPE55 |
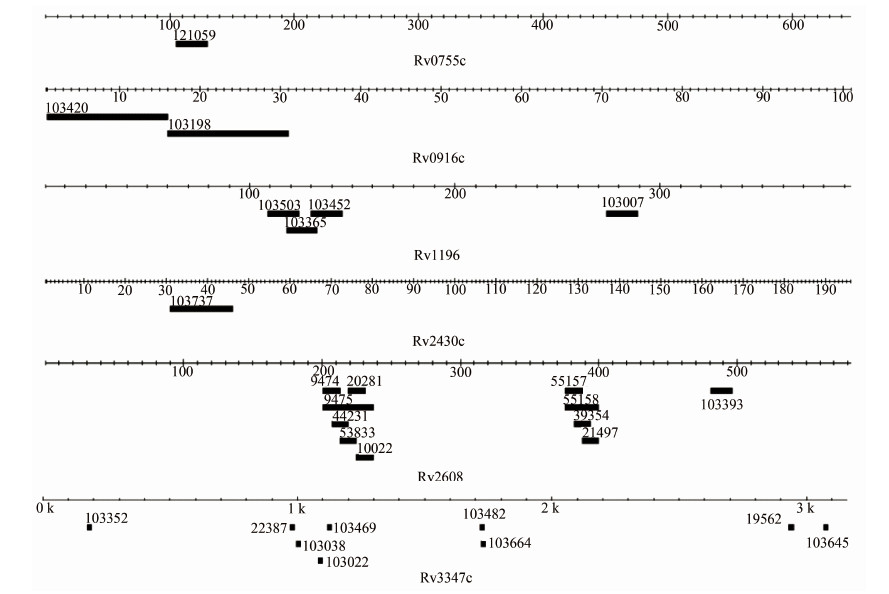
其中基因Rv0755c编码蛋白PPE12,分布1个B细胞抗原表位;基因Rv0916c编码蛋白PE7,分布2个B细胞抗原表位;基因Rv1196编码蛋白PPE18,分布4个B细胞抗原表位;基因Rv2430c编码蛋白PPE41,分布1个B细胞抗原表位;基因Rv2608编码蛋白PPE42,分布11个B细胞抗原表位;基因Rv3347c编码蛋白PPE55,分布9个B细胞抗原表位。不同PE/PPE家族蛋白中B细胞抗原表位的分布见图 2。
|
| 图2 PE/PPE家族蛋白中B细胞抗原表位的分布 Figure 2 Distribution of B cell epitopes in PE/PPE protein family |
将PE/PPE基因家族中编码B细胞抗原表位的核酸序列与13株BCG、1株牛结核分枝杆菌的全基因组进行序列比对,提取核酸编码序列。28个PE/PPE基因家族编码的B细胞抗原表位中,7个抗原表位(编号103007、103365、103503、103038、103352、22387、103737)的编码序列呈现不同程度的变化,21个抗原表位的编码序列在13株BCG中呈现高度保守。
与M.tb H37Rv基因组相比,7个存在碱基变化的B细胞抗原表位中,5个抗原表位(编号103007、103365、103503、103038、103352)的编码序列在13株BCG中均存在相同点突变,1个抗原表位(编号22387)的编码序列在4株BCG中存在相同的点突变,1个抗原表位(编号103737)编码序列在1株BCG基因组中存在碱基缺失。在13株BCG中,抗原表位103007的编码序列上存在3个点突变,其中2个位点为同义突变,1个位点为错义突变;抗原表位103365在13株BCG中均存在相同的错义突变;抗原表位103503在13株BCG中存在相同的错义突变;抗原表位103737在BCG-Moreau中存在单碱基缺失;抗原表位22387在菌株BCG-Phipps、BCG-Prague、BCG-Russia和BCG-Tice中相同位置存在点突变;抗原表位103038在13株BCG基因组中存在相同位置的2个同义突变;抗原表位103352在13株BCG基因组中存在相同位置的1个错义突变。
与M.bovis AF2122/97基因组相比,3个B细胞抗原表位(编号103007、103352、103038)的编码序列在M.bovis AF2122/97基因组中存在不同程度变化,且序列变化与在BCG基因组中的变化一致;其余25个B细胞抗原表位编码序列未发生变化。见表 3、4。
| 编号 | 103007 | 103365 | 103503 | 103737 | 22387 | 103038 | 103352 |
| M.tb H37Rv | - | - | - | - | - | - | - |
| M.bovis AF2122/97 | + | - | - | - | - | + | + |
| BCG-Moreau | + | + | + | + | - | + | + |
| BCG-Swedens | + | + | + | - | - | + | + |
| BCG-Phipps | + | + | + | - | + | + | + |
| BCG-China | + | + | + | - | - | + | + |
| BCG-Danish | + | + | + | - | - | + | + |
| BCG-Prague | + | + | + | - | + | + | + |
| BCG-Russia | + | + | + | - | + | + | + |
| BCG-Tice | + | + | + | - | + | + | + |
| BCG-Glaxo | + | + | + | - | - | + | + |
| BCG-Mexico | + | + | + | - | - | + | + |
| BCG-Pasteur | + | + | + | - | - | + | + |
| BCG-Tokyo 172 | + | + | + | - | - | + | + |
| BCG-Frappier | + | + | + | - | - | + | + |
| 注:“+”存在基因改变,“-”未存在基因改变。 | |||||||
| 编号 | 核酸序列变化 | 氨基酸序列变化 |
| 103007 | 3:C-G;6:C-T;16:C-G | A-A;A-A;Q-E |
| 103365 | 14-15:TA-CC | I-T |
| 103503 | 41-42:TA-CC | I-T |
| 103737 | 25:缺失 | 移码突变 |
| 22387 | 33:C-T | G-G |
| 103038 | 34:T-C;42:A-G | L-L;R-R |
| 103352 | 34:C-A | L-I |
基因Rv0755c、Rv0916c、Rv2608所编码的14个B细胞抗原表位在13株BCG以及菌株M.bovis AF2122/97高度保守。
Rv1196基因编码4个B细胞抗原表位,其中3个B细胞抗原表位在13株BCG中均出现相同的基因改变、1个B细胞抗原表位未发生变异;在M.bovis AF2122/97基因组中1个B细胞抗原表位发生变异且与在BCG中变化相同、其他3个B细胞抗原表位未发生变化。
Rv2430c基因编码1个B细胞抗原表位,在1株BCG中发生碱基缺失现象,在其他BCG菌株以及M.bovis AF2122/97中高度保守。
基因Rv3347c编码9个B细胞抗原表位,其中1个B细胞抗原表位在4株BCG中存在变异、在其他BCG菌株以及M.bovis AF2122/97中高度保守,2个B细胞抗原表位在BCG菌株和M.bovis AF2122/97中均发生基因改变,其余6个B细胞抗原表位在所有菌株中高度保守。
3 讨论TB是一种古老的疾病,人类与TB的抗争贯穿着整个文明史[21]。TB的肆虐不仅危害着人类的健康,而且对全球经济的正常运行造成了严重影响[22]。BCG可以有效地预防儿童TB,但对成人防治效果不明显,且BCG的免疫保护效果也因不同地区、不同种族等原因存在显著差异。尽管不断有报道称新型结核疫苗处于研发状态或是临床试验阶段,但迄今为止BCG仍然是市场上唯一获准广泛用于预防TB的疫苗。
BCG是一种减毒活疫苗。现在全球范围内应用的BCG主要经历了两个形成阶段。第一阶段,从19081921年将牛结核分枝杆菌连续进行传代培养后获得了原始BCG菌株;在这个阶段BCG丢失了基因组中多个重要基因并形成了一些基因变异。第二阶段,从1924年开始BCG扩散到全球多个国家,随后的几十年中BCG在不同国家被广泛应用并成了地域性克隆,克隆依据使用的地域命名,例如BCG-China、BCG-Danish、BCG-Russia等。地域性的BCG在传代培养过程中产生了各自特异性基因变异[3]。变异模式持续到1966年,WHO规定用做疫苗的菌株连续传种不能超过12代。而此时大多数BCG已经在不同国家至少传代培养了1000代以上,且由于BCG减毒机制不是十分清楚,形成了多个拥有不同保护性抗原、理化性质、免疫特征、甚至是不同表型的BCG克隆[23, 24, 25]。
本研究的结果显示,与结核分枝杆菌基因组相比,BCG中7个由PE/PPE基因家族编码的B细胞抗原表位在基因水平发生了变异。其中抗原表位103007、103352和103038在BCG和M.bovis基因组中均呈现一致性变异,推测这类变异为牛结核分枝杆菌基因组固有,不同BCG菌株基因组中的此类变异来源于原始BCG菌株。抗原表位103365和103503的编码序列在BCG菌株中检测到碱基改变,而在M.bovis基因组中未检测到同样的变化,推测此类变化发生于19081921年,原始BCG菌株发生了基因序列的改变并遗传至子代BCG中。而抗原表位103737和22387编码序列中的基因变异只存在于少数几个BCG菌株中,在M.bovis基因组中未发现同样的变化,可能是由于从19241966年间,原始BCG菌株在不同的国家或地区传播所面临的不同选择性压力导致。
造成接种BCG后产生不同保护效力的原因目前仍然不是十分清楚,但已经提出了很多假设对此做出解释,主要包括不同临床试验中BCG菌株选择的差异、接种BCG的人群可能同时受环境中分枝杆菌属其他细菌的感染、接种人群本身的遗传特征差异、临床试验方法的不同以及BCG本身存在差异等[3, 26, 27, 28]。这其中比较重要的原因就是人群中接种的BCG形成过程不同造成不同疫苗株之间存在较大差异。从PE/PPE基因家族编码的B细胞抗原表位分析,在13株BCG中,6个B细胞抗原表位的编码序列在BCG-Moreau中发生了改变导致其中5个B细胞抗原表位随之发生了改变;在BCG-Phipps、BCG-Prague、BCG-Russia和BCG-Tice中,6个B细胞抗原表位的编码序列发生了改变导致4个B细胞抗原表位发生了变异;在其他8株BCG中,5个B细胞抗原表位的编码序列发生改变导致4个B细胞抗原表位发生了变异。因此在BCG-Moreau基因组中,PE/PPE基因家族编码数量最少的B细胞抗原表位,可能会导致将其应用于人群后所产生的免疫保护力与其他BCG相比有所变化。
目前PE/PPE家族蛋白的结构和功能不十分清楚,但已有研究表明PE/PPE家族蛋白与细菌毒力有关、在细菌免疫逃逸和抗原变异性中起作用[29]。基因Rv0755c、Rv0916c和Rv2608编码14个B细胞抗原表位,在13株BCG中高度保守。基因Rv1196编码蛋白PPE18,可以刺激宿主免疫系统分泌细胞因子调节免疫应答[30];基因Rv2430c编码蛋白PPE41,与PPE25形成复合物可以显著增强B细胞免疫应答[31];基因Rv3347c编码蛋白PPE55,可以作为新型结核疫苗的备选成分,用于区分结核的潜伏感染[32]。因此上述基因中出现的序列变异所导致的B细胞抗原表位变化,可能会影响到宿主免疫系统对结核分枝杆菌的识别与清除作用、抑制宿主的免疫应答。
本研究中对B细胞抗原表位在BCG中的分布进行分析,PE/PPE基因家族编码B细胞抗原表位中发生的变异产生于BCG菌株的不同形成期,其分布可能影响宿主免疫系统对结核分枝杆菌免疫应答。虽然本研究首次采用B细胞表位研究其分布状态对PE/PPE基因及抗结核免疫可能存在的影响,但也存在不足。首先,本研究所关注的28个表位,仅占全部已知表位的一部分,其代表性尚存在一定的争议;其次,已发表的研究多关注结核的细胞免疫反应,因此在IEDB中经验证的B细胞表位数量较少,因此在结核分枝杆菌及PE/PPE蛋白家族中可能存在更多的免疫表位会对宿主与病原之间的相互作用产生影响;第三,目前对PE/PPE基因家族及其表达产物的功能与作用机制尚不十分清楚,因此对B细胞表位的研究也存在局限性。综上所述,在后续的研究中将对全部经过试验验证的B细胞抗原表位进行分析,并结合生物信息学预测的模式,对已有表位及预测表位采用体外血清学检测、基因缺失/回补、转录表达谱等方式进行相应的免疫学验证试验来了解BCG菌株之间的遗传特征差异。
| [1] | Vashishtha VM. WHO Global Tuberculosis Control Report 2009: Tuberculosis elimination is a distant dream[J]. Indian Pediatr,2009,46(5):401-402. |
| [2] | Technical Guidance Group of the Fifth National TB EpidemiologicalSurvey, The Office of the Fifth National TB Epidemiological Survey. The fifth national tuberculosis epidemiological survey in 2010[J]. Chinese Journal of Antituberculosis,2012,34(8):485-508. (in Chinese) 全国第五次结核病流行病学抽样调查技术指导组, 全国第五次结核病流行病学抽样调查办公室. 2010年全国第五次结核病流行病学抽样调查报告[J]. 中国防痨杂志,2012,34(8):485-508. |
| [3] | Liu JTV, Tran V, Leung AS, et al. BCG vaccines: their mechanisms of attenuation and impact on safety and protective efficacy[J]. Hum Vaccin,2009,5(2):70-78. |
| [4] | Olle Goig JE.[Expanded programme on immunization]El programa ampliado de vacunacion[J]. Med Clin,1989,93(10):383-386. |
| [5] | Milstien JB, Gibson JJ. Quality control of BCG vaccine by WHO: a review of factors that may influence vaccine effectiveness and safety[J]. Bull World Health Organ, 1990, 68(1):93-108. |
| [6] | Maglione PJ, Xu JY, Chan J. B cells moderate inflammatory progression and enhance bacterial containment upon pulmonary challenge with Mycobacterium tuberculosis[J]. J Immunol,2007,178(11):7222-7234. |
| [7] | Maglione PJ, Xu JY, Casadevall A, et al. Fcγ receptors regulate immune activation and susceptibility during Mycobacterium tuberculosis infection[J]. J Immunol,2008,180(5):3329-3338. |
| [8] | Ulrichs T, Kosmiadi GA, Trusov V, et al. Human tuberculous granulomas induce peripheral lymphoid follicle-like structures to orchestrate local host defence in the lung[J]. J Pathol,2004,204(2):217-228. |
| [9] | Cole ST, Brosch R, Parkhill J, et al. Deciphering the biology of Mycobacterium tuberculosis from the complete genome sequence[J]. Nature,1998,393(6685):537-544. |
| [10] | Banu S, Honoré N, Saint-Joanis B, et al. Are the PE-PGRS proteins of Mycobacterium tuberculosis variable surface antigens?[J]. Mol Microbiol,2002,44(1):9-19. |
| [11] | Delogu G, Pusceddu C, Bua A, et al. Rv1818c-encoded PE_PGRS protein of Mycobacterium tuberculosis is surface exposed and influences bacterial cell structure[J]. Mol Microbiol,2004,52(3):725-733. |
| [12] | Delogu G, Brennan MJ. Comparative immune response to PE and PE_PGRS antigens of Mycobacterium tuberculosis[J]. Infect Immun,2001,69(9):5606-5611. |
| [13] | Zhang W, Zhang YY, Zheng HJ, et al. Genome sequencing and analysis of BCG vaccine strains[J]. PLoS One,2013,8(8):e71243. |
| [14] | Pan YL, Yang X, Duan J, et al. Whole-genome sequences of four Mycobacterium bovis BCG vaccine strains[J]. J Bacteriol, 2011,193(12):3152-3153. |
| [15] | Ordua P, Cevallos MA, de León SP, et al. Genomic and proteomic analyses of Mycobacterium bovis BCG Mexico 1931 reveal a diverse immunogenic repertoire against tuberculosis infection[J]. BMC Genomics,2011,12(1):493. |
| [16] | Brosch R, Gordon SV, Garnier T, et al. Genome plasticity of BCG and impact on vaccine efficacy[J]. Proc Natl Acad Sci USA,2007,104(13):5596-5601. |
| [17] | Seki M, Honda I, Fujita I, et al. Whole genome sequence analysis of Mycobacterium bovis bacillus Calmette-Guérin (BCG) Tokyo 172: a comparative study of BCG vaccine substrains[J]. Vaccine,2009,27(11):1710-1716. |
| [18] | Camus JC, Pryor MJ, Médigue C, et al. Re-annotation of the genome sequence of Mycobacterium tuberculosis H37Rv[J]. Microbiology,2002,148(Pt 10):2967-2973. |
| [19] | Garnier T, Eiglmeier K, Camus JC, et al. The complete genome sequence of Mycobacterium bovis[J]. Proc Natl Acad Sci USA,2003,100(13):7877-7882. |
| [20] | Kent WJ. BLAT-the BLAST-like alignment tool[J]. Genome Res,2002,12(4):656-664. |
| [21] | Daniel TM. The history of tuberculosis[J]. Respir Med,2006,100(11):1862-1870. |
| [22] | Jack W. The public economics of tuberculosis control[J]. Health Policy,2001,57(2):79-96. |
| [23] | Fine PEM, Carneiro IAM, Milstien JB, et al. Issues relating to the use of BCG in immunization programmes:a discussion document[R]. Geneva: World Health Organization, 1999. |
| [24] | Bunch-Christensen K, Ladefoged A, Guld J. The virulence of some strains of BCG for golden hamsters[J]. Bull World Health Organ,1968,39(1):821-828. |
| [25] | Lagranderie MR, Balazuc AM, Deriaud E, et al. Comparison of immune responses of mice immunized with five different Mycobacterium bovis BCG vaccine strains[J]. Infect Immun, 1996, 64(1):1-9. |
| [26] | Fine PEM. Variation in protection by BCG: implications of and for heterologous immunity[J]. Lancet, 1995, 346(8986):1339-1345. |
| [27] | Sadeghi-Shabestari M, Vesal S, Jabbarpour-Bonyadi M, et al. Novel RAG2 mutation in a patient with T-B-severe combined immunodeficiency and disseminated BCG disease[J]. J Investig Allergol Clin Immunol,2009,19(6):494-496. |
| [28] | Marchand I, Mahé E, Clérici T, et al. Disseminated BCG infection revealing X-linked severe combined immunodeficiency[J]. Ann Dermatol Vénéréol,2008,135(8/9):587-590. |
| [29] | Ramakrishnan L, Federspiel NA, Falkow S. Granuloma-specific expression of Mycobacterium virulence proteins from the glycine-rich PE-PGRS family[J]. Science,2000,288(5470):1436-1439. |
| [30] | Nair S, Pandey AD, Mukhopadhyay S. The PPE18 protein of Mycobacterium tuberculosis inhibits NF-κB/rel-mediated proinflammatory cytokine production by upregulating and phosphorylating suppressor of cytokine signaling 3 protein[J]. JImmunol,2011,186(9):5413-5424. |
| [31] | Tundup S, Akhter Y, Thiagarajan D, et al. Clusters of PE and PPE genes of Mycobacterium tuberculosis are organized in operons: Evidence that PE Rv2431c is co-transcribed with PPE Rv2430c and their gene products interact with each other[J]. FEBS Lett,2006,580(5):1285-1293. |
| [32] | Zvi A, Ariel N, Fulkerson J, et al. Whole genome identification of Mycobacterium tuberculosis vaccine candidates by comprehensive data mining and bioinformatic analyses[J]. BMC Med Genomics,2008,1(1):18. |
 2016, Vol. 31
2016, Vol. 31


