扩展功能
文章信息
- 周俊英, 乐英棒
- ZHOU Jun-ying, YUE Ying-bang
- 重症监护病房耐甲氧西林金黄色葡萄球菌基因同源性分析
- Gene homology analysis on methicillin resistant Staphylococcus aureus isolated in intensive care unit
- 疾病监测, 2017, 32(12): 958-961
- Disease Surveillance, 2017, 32(12): 958-961
- 10.3784/j.issn.1003-9961.2017.12.015
-
文章历史
- 收稿日期:2017-07-19
金黄色葡萄球菌是引起医院感染的重要致病菌,其中重症监护病房(intensive care unit,ICU)是耐甲氧西林的金黄色葡萄球菌(methicillin-resistant Staphylococcus aureus,MRSA)感染的重灾区[1]。MRSA医院感染可能来自于医生和护士的手、物品、水和空气等环境中的病原体,由于ICU患者病情危重、住院时间长及一些侵入性操作等因素,其获得MRSA医院感染的可能性大且危险性高[2]。ICU患者多为其他病房甚至外院转来的危重患者,病情缓解稳定后需转出ICU至其他病房,导致其在医院MRSA的播散上起到重要作用。
本实验主要通过对武汉大学中南医院ICU患者的标本与医院ICU医务人员手及环境表面进行MRSA的分离鉴定和耐药检测,并运用肠杆菌基因间重复共有序列聚合酶链反应(enterobacterial repetitive intergenic consensus polymerase chain reaction,ERIC-PCR)技术对MRSA基因分型,分析MRSA的同源性。
1 材料与方法 1.1 临床菌株收集2016年3-12月武汉大学中南医院ICU病房分离出的金黄色葡萄球菌,共33株;采集ICU环境标本41份,包括医生护士的手、桌面、电脑键盘、鼠标、病历本、门把手、换药室桌面、水龙头、床架、床头桌、床单、呼吸机、听诊器以及空气等。
1.2 质控菌株金黄色葡萄球菌标准菌株ATCC25923和ATCC29213。
1.3 试剂和仪器血平板由广州迪景微生物科技有限公司提供,MH琼脂和药敏纸片由英国OXOID公司提供,ERIC引物由上海生工公司合成,TaqDNA聚合酶和dNTPs由Fermantas公司提供,DNA Marker由HBI公司提供,PCR扩增仪为MJ Research Inc公司的PTC-200 PCR仪,TGL-16K高速离心机、Mini UV-1微型紫外投射仪均由珠海黑马医学仪器有限公司提供,POWER PAC 3000型电泳仪由美国BIO-RAD公司提供。
1.4 实验方法 1.4.1 细菌的分离和鉴定按《全国临床检验操作规程》进行[3],药敏试验采用K-B法。
1.4.2 引物序列ERIC1序列:ATG TAA GCT CCT GGG GAT TCA C;ERIC2序列:AAG TAA GTG ACT GGG GTG AGC G。
1.4.3 细菌DNA模板制备按实验室常规的酚/氯仿法提取。
1.4.4 ERIC-PCR反应体系总体积20 μl,包括模板DNA为2 μl,10×PCR缓冲液2 μl,MgCl2 25 mmol/L 1.2 μl,dNTP (10 mmol/L)1 μl,Taq DNA聚合酶(5 U/μl)1 μl,ERIC1和ERIC2各2 μl,双蒸水8.8 μl。
1.4.5 反应条件循环参数:94 ℃ 5 min预变性,94 ℃变性1 min,52 ℃退火1 min,72 ℃延伸4 min,共30个反应循环,最后72 ℃ 10 min。PCR反应产物采1.5 g/L琼脂糖凝胶(1×TBE)电泳,电压100 V,电泳10 min,紫外灯下判读结果
1.5 聚类分析将ERIC-PCR电泳谱带数据转换成矩阵,用0和1代表谱带的无和有,然后运用NTSYS-PC 2.0软件对21株MRSA扩增产物进行相似性分析,聚类分法选用非加权组平均法(unweighted pair-group method with arithmetic means,UPGMA)。
2 结果 2.1 细菌鉴定结果采集ICU医务人员手及环境表面中标本共41份,分离出金黄色葡萄球菌6株,其中5株为MRSA,检出率为12.19%,分别来自桌面、医护人员手、不同房间的空气和床单;ICU患者标本中共分离出33株金黄色葡萄球菌,16株为MRSA,占金黄色葡萄球菌检出率为48.5%,这16株病例中,男性10例,女性6例,15株来自肺部感染,1株来自腹腔引流液。
2.2 药敏实验16株MRSA临床患者分离株中,所有菌株对万古霉素、利奈唑胺、替考拉宁敏感,耐药率为0%,MRSA菌株对青霉素、苯唑西林和头孢西丁耐药率为100%,环丙沙星、红霉素、克林霉素、左氧氟沙星、庆大霉素、妥布霉素耐药率分别为93.75%、81.25%、75.00%、87.50%、62.50%、50.00%,复方新诺明和氯霉素耐药率相对较低,分别为31.25%和18.75%。
ICU环境标本分离出5株MRSA,其对氯霉素、万古霉素、利奈唑胺、替考拉宁、妥布霉素耐药率为0,对青霉素、环丙沙星、左氧氟沙星耐药率为100%,对青霉素、环丙沙星、左氧氟沙星、苯唑西林、红霉素呈高度耐药,耐药率>80%,对复方新诺明、庆大霉素、克林霉素也产生了较高的耐药性,耐药率>40%,见表 1。
| 药物名称 | 患者标本耐药率(%) | 环境标本耐药率(%) |
| 头孢西丁(FOX) | 100.00(16/16) | 100.00(5/5) |
| 复方新诺明(SXT) | 31.25(5/16) | 60.00(3/5) |
| 青霉素(P) | 100.00(16/16) | 100.00(5/5) |
| 氯霉素(C) | 18.75(3/16) | 0.00(0/5) |
| 左氧氟沙星(LEV) | 87.50(14/16) | 100.00(5/5) |
| 庆大霉素(CN) | 62.50(10/16) | 40.00(2/5) |
| 环丙沙星(CIP) | 93.75(15/16) | 100.00(5/5) |
| 万古霉素(VA) | 0.00(0/16) | 0.00(0/5) |
| 苯唑西林(OX) | 100.00(16/16) | 100.00(5/5) |
| 利奈唑胺(LZD) | 0.00(0/16) | 0.00(0/5) |
| 克林霉素(DA) | 75.00(12/16) | 40.00(2/5) |
| 红霉素(E) | 81.25(13/16) | 80.00(4/5) |
| 替考拉宁(TEC) | 0.00(0/16) | 0.00(0/5) |
| 妥布霉素(TOB) | 50.00(8/16) | 0.00(0/5) |
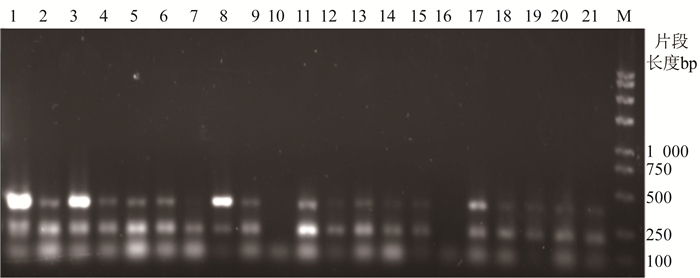
采用ERIC-PCR方法对5株环境标本分离出的MRSA和16株ICU患者标本分离出的MRSA以及质控菌株进行基因分析。1~16为患者标本分离株,17~21为环境分离株,电泳结果显示最大的分子质量约为450 bp,最小的分子质量约为100 bp,见图 1。
|
| 图 1 21株金黄色葡萄球菌ERIC-PCR检测电泳结果 Figure 1 ERIC-PCR electrophoresis results of 21 strains of S. aureus 注:M:Marker; 1~16为患者标本分离株;17~21为环境分离株 |
| |
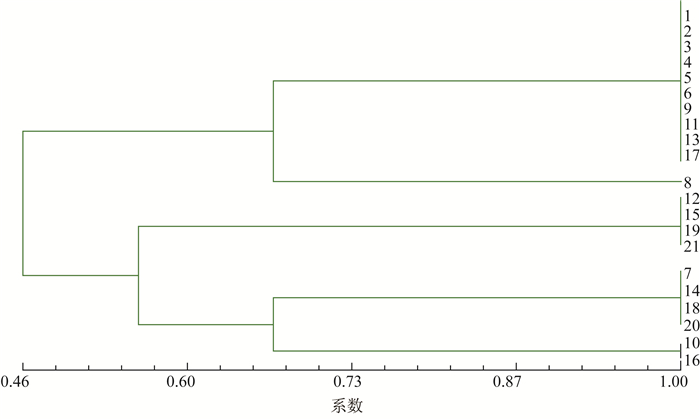
运用NTSYS-PC 2.0软件对21株MRSA扩增产物进行相似性分析,21株菌的DNA同源性在46.00%~67.00%之间。同源性在68.00%时可分为3类。菌株第1、2、3、4、5、6、9、11、13、17、8为一类,菌株第12、15、19、21为一类,菌株第7、14、18、20、10、16为一类,菌株第1、2、3、4、5、6、9、11、13、17亲缘关系较近,菌株第12、15、19、21亲缘关系较近,菌株第7、14、18、20亲缘关系较近,相关性达90.00%,特别是在第一类中,有9株是痰培养,1株为实习生的手部细菌培养,相似度极高,见图 2。
|
| 图 2 ERIC-PCR结果聚类分析 Figure 2 Cluster analysis of ERIC-PCR results |
| |
MRSA是ICU内发生高患病率及高死亡率的重要病因,MRSA大部分表现为多重耐药,不仅对β-内酰胺类抗菌药耐药,还对喹诺酮类、氨基苷类和大环内酯类等抗菌药物耐药。万古霉素被认为是治疗MRSA感染的最后一道防线,但近几年又发现了对万古霉素中介或耐药的MRSA[4],给临床治疗MRSA感染带来了极大的困难。
本实验从ICU环境标本分离出5株MRSA,分别来自桌面、ICU医护人员手、2份空气标本和ICU床单,对氯霉素、万古霉素、利奈唑胺等耐药率为0%,对青霉素、环丙沙星等呈高度耐药,耐药率>80.00%,这说明ICU环境中存在较为严重的多重耐药MRSA,为控制医院感染,应加强病房环境微生物监测,定期对医务人员的手、物体表面、空气等进行细菌学监测,加强消毒隔离措施,严格执行无菌技术操作,特别是手卫生规范的执行,及时采取预防控制措施。
ICU临床标本分离的16株MRSA对万古霉素、利奈唑胺、替考拉宁完全敏感,对青霉素、环丙沙星等多种抗生素呈高度耐药,耐药率>80.00%,这表明ICU的MRSA多重耐药现象比较严重,临床医生应正确合理使用抗菌药物,延缓或减少耐药菌株的产生,保证正确、有效的临床治疗。
MRSA是引起医院感染的重要致病菌之一[5-6],国内外均有报道ICU环境分离出MRSA,且与临床分离标本有高度同源性,说明他们可能来自同一菌株的播散。
从药敏实验结果和耐药表型分析,ICU环境标本与临床分离标本有一定的表型同源性,但不完全一致。它们对青霉素、环丙沙星、苯唑西林、红霉素都呈高度耐药;但环境菌株对氯霉素、妥布霉素敏感,临床分离菌株却呈现不同程度的耐药;环境菌株对复方新诺明耐药,而临床分离菌株对复方新诺明耐药率却较低。运用ERIC-PCR基因分型结果显示:ICU医生的手分离出的17号菌株与环境分离第1、2、3、4、5、6、7、9、11、13共9株MRSA有相同的条带,特别是在前一类中,有9株是肺部感染患者分离株,1株为实习生的手部细菌培养,相似度极高,说明有可能来自同一传染源,医护人员特别是实习生手部卫生依从性较差,是造成局部感染流行的主要原因。因此必须加强ICU全体工作人员消毒隔离知识的培训,严格做到在接触患者和诊疗操作前后进行洗手或手消毒,彻底清洁和消毒可能被病原体污染的环境表面和设备,专人负责层流空气净化系统的日常保养,彻底清洗回风口过滤网,同时制定层流病房空气净化系统管理制度,定期更换过滤器或根据空气培养的结果增加更换次数,以确保层流病房空气洁净,从而达到减缓并控制ICU耐药菌局部流行。
作者贡献:
周俊英 ORCID:0000-0002-4698-1401
周俊英:主要负责耐甲氧西林金黄色葡萄球菌的同源性分析
乐英棒:负责收集菌株、药敏试验及临床资料整理
| [1] |
Chen Q, Jin H, Xu H, et al. Distribution of methicillin-resistant Staphylococcus aureus strains isolated from ICU[J]. Chinese Journal of Nosocomiology, 2016, 26(11): 2447-2449. (in Chinese) 陈琦, 金慧, 徐虹, 等. ICU耐甲氧西林金黄色葡萄球菌分布特征分析[J]. 中华医院感染学杂志, 2016, 26(11): 2447-2449. |
| [2] |
Shi XY, Chen QR, Yu XY, et al. Rapid monitoring and prevention of methicillin-resistant Staphylococcus aureus in ICU[J]. International Journal of Laboratory Medicine, 2015, 36(7): 877-879. (in Chinese) 史小英, 陈启容, 余新玉, 等. ICU耐甲氧西林金黄色葡萄球菌快速监测及防控[J]. 国际检验医学杂志, 2015, 36(7): 877-879. |
| [3] |
Shang H, Wang YS, Shen ZY. National laboratory operating procedure[M]. 4th ed. Beijing: People's Medical Publishing House, 2015: 648-653. (in Chinese) 尚红, 王毓三, 申子瑜. 全国临床检验操作规程[M]. 4版. 北京: 人民卫生出版社, 2015: 648-653. |
| [4] |
Zarpellon MN, Gales AC, Sasaki AL, et al. Survival of vancomycin-intermediate Staphylococcus aureus on hospital surfaces[J]. J Hosp Infect, 2015, 90(4): 347-350. DOI:10.1016/j.jhin.2015.04.005 |
| [5] |
Zhu JQ, Jiang Y. Drug resistance of Staphylococcus aureus in 2011[J]. Chinese Journal of Nosocomiology, 2013, 23(6): 1428-1430. (in Chinese) 诸军权, 蒋银. 2011年金黄色葡萄球菌耐药性分析[J]. 中华医院感染学杂志, 2013, 23(6): 1428-1430. |
| [6] |
Liu Z, Yang K, Yao J, et al. Antimicrobial resistance and clinical epidemic trend of Staphylococcus aureus[J]. Acta Universitatis Medicinalis Anhui, 2013, 48(4): 409-412. (in Chinese) 刘周, 杨凯, 姚杰, 等. 金黄色葡萄球菌临床流行趋势及耐药性分析[J]. 安徽医科大学学报, 2013, 48(4): 409-412. |
 2017, Vol. 32
2017, Vol. 32


